
 .
.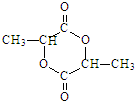 .
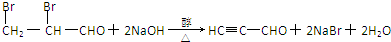
. 分析 有机化合物A经李比希法测得其中含碳 64.3%、含氢7.1%,其余为氧,经质谱法分析得知其相对分子质量为56,则A中含有C原子数为$56×\frac{64.3%}{12}$=3,H原子数为$56×\frac{7.1%}{1}$=4,O原子数为$56×\frac{1-64.3%-7.1%}{16}$=1,所以A的分子式为C3H4O,经核磁共振氢谱确定分子中有3种不同化学环境的氢原子,A能与Br2的CCl4溶液反应,且能发生银镜反应,则A为CH2=CHCHO,A与Br2的CCl4溶液发生加成反应生成B为BrCH2CHBrCHO,B与NaOH的醇溶液共热生成C,C的相对分子质量为54,则C为CH≡CCHO,A与银氨溶液反应得到D为CH2=CHCOONH4,D经酸化后可与HCl加成得到E含有氯原子,E与NaOH的水溶液共热,氯原子被羟基取代,反应后再酸化得到F,F在浓硫酸作用下发生酯化反应,生成一种六元环状化合物G,则可推知E为CH3CHClCOOH,F为CH3CHOHCOOH,G为 ,据此答题.
,据此答题.
解答 解:有机化合物A经李比希法测得其中含碳 64.3%、含氢7.1%,其余为氧,经质谱法分析得知其相对分子质量为56,则A中含有C原子数为$56×\frac{64.3%}{12}$=3,H原子数为$56×\frac{7.1%}{1}$=4,O原子数为$56×\frac{1-64.3%-7.1%}{16}$=1,所以A的分子式为C3H4O,经核磁共振氢谱确定分子中有3种不同化学环境的氢原子,A能与Br2的CCl4溶液反应,且能发生银镜反应,则A为CH2=CHCHO,A与Br2的CCl4溶液发生加成反应生成B为BrCH2CHBrCHO,B与NaOH的醇溶液共热生成C,C的相对分子质量为54,则C为CH≡CCHO,A与银氨溶液反应得到D为CH2=CHCOONH4,D经酸化后可与HCl加成得到E含有氯原子,E与NaOH的水溶液共热,氯原子被羟基取代,反应后再酸化得到F,F在浓硫酸作用下发生酯化反应,生成一种六元环状化合物G,则可推知E为CH3CHClCOOH,F为CH3CHOHCOOH,G为 ,
,
(1)根据上面的分析可在,A的分子式是C3H4O,A为CH2=CHCHO,分子中的官能团名称是碳碳双键、醛基,A→B所属反应类型是加成反应,
故答案为:C3H4O;碳碳双键、醛基;加成反应;
(2)B→C的化学方程式是 ,
,
故答案为: ;
;
(3)A→D的化学方程式是 CH2=CH-CHO+2Ag(NH3)2OH$\frac{\underline{\;\;△\;\;}}{\;}$CH2=CH-COONH4+2Ag↓+3NH3+H2O,
故答案为:CH2=CH-CHO+2Ag(NH3)2OH$\frac{\underline{\;\;△\;\;}}{\;}$CH2=CH-COONH4+2Ag↓+3NH3+H2O;
(4)根据上面的分析可知,G的结构简式是 ,
,
故答案为: .
.
点评 本题考查了有机物分子式、结构简式的确定,题目难度中等,明确核磁共振氢谱、质谱法的含义为解答关键,注意根据官能团的性质及相互转化进行物质推断,试题培养了学生的分析、理解能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA | |
| B. | 高温下,0.3molFe与足量水蒸气反应,生成的H2的体积为8.96L | |
| C. | 1mol Na2O2固体中含离子总数为4 NA | |
| D. | 标准状况下6.72 L NO2与水反应转移的电子数0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高铁酸钠中铁显+6价 | |
| B. | 湿法中每生成1 mol Na2FeO4转移3 mol电子 | |
| C. | 干法中每生成1 mol Na2FeO4转移3 mol电子 | |
| D. | Na2FeO4处理水时,不仅能消毒杀菌,还能除去水体中的H2S、NH3等,生成的Fe(OH)3还能吸附水中的悬浮杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
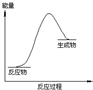
| A. | 氢气与氧气反应生成液态水 | |
| B. | 稀盐酸与金属镁反应 | |
| C. | 生石灰与稀盐酸反应 | |
| D. | 硫酸铵晶体与氢氧化钡晶体混合研磨而反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| B. | SiO2 是酸性氧化物,能与NaOH溶液反应 | |
| C. | Na2O、Na2O2组成元素相同,与 CO2反应产物也相同 | |
| D. | SO2和新制氯水均有漂白性,将SO2和Cl2通入滴加少量紫色石蕊试液,充分振荡后溶液最终呈无色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{m}{64}$ g | B. | $\frac{48m}{32}$$\frac{49m}{32}$g | C. | $\frac{n}{22.4}$mol | D. | 不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
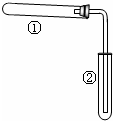 如图装置(夹持、加热装置已略)进行实验,有②中现象,不能证实①中反应发生的是( )
如图装置(夹持、加热装置已略)进行实验,有②中现象,不能证实①中反应发生的是( )| ①中实验 | ②中现象 |
| 铁粉与水蒸气加热 | 肥皂水冒泡 |
| 加热NH4Cl和Ca(OH)2混合物 | 酚酞溶液变红 |
| NaHCO3 | 澄清石灰水变浑浊 |
| 石蜡油在碎瓷片上受热分解 | Br2的CCl4溶液褪色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com