
| A. | 滴加酚酞后溶液均变红 | |
| B. | 滴加饱和澄清石灰水均产生白色沉淀 | |
| C. | 滴加氯水均产生能使澄清石灰水变浑浊的气体 | |
| D. | 所含阳离子的总浓度相等 |
分析 A、NaHSO3溶液电离程度大于水解程度,所以溶液呈酸性;
B、NaHCO3溶液与氢氧化钙反应生成碳酸钙和NaHSO3溶液与氢氧化钙反应生成亚硫酸钙沉淀;
C、NaHSO3溶液滴加氯水发生氧化还原反应生成硫酸钠;
D、阳离子为钠离子与氢离子,相同物质的量浓度的NaHCO3溶液和NaHSO3溶液,所以钠离子总数相等,而氢离子总数不等.
解答 解:A、NaHSO3溶液电离程度大于水解程度,所以溶液呈酸性,所以NaHSO3滴加酚酞后溶液不变红,故A错误;
B、NaHCO3溶液与氢氧化钙反应生成碳酸钙和NaHSO3溶液与氢氧化钙反应生成亚硫酸钙沉淀,所以滴加饱和澄清石灰水均产生白色沉淀,故B正确;
C、NaHSO3溶液滴加氯水发生氧化还原反应生成硫酸钠,而无气体产生,故C错误;
D、阳离子为钠离子与氢离子,相同物质的量浓度的NaHCO3溶液和NaHSO3溶液,所以钠离子总数相等,而亚硫酸氢钠电离子程度大于水解程度,碳酸钠水解程度大于电离程度,所以亚硫酸氢钠氢离子总数大,所以两者所含阳离子的总浓度不相等,故D错误;
故选B.
点评 本题考查钠的化合物的性质,学生要注意亚硫酸氢钠电离程度大于水解程度,注意对基础知识的理解掌握,有一定的难度.


科目:高中化学 来源: 题型:选择题
| A. | 醋酸与氢氧化钠溶液反应:OH-+H+═H2O | |
| B. | 氯气与水反应:Cl2+H2O?Cl-+HClO+H+ | |
| C. | 铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ | |
| D. | 氢氧化钡溶液与稀H2SO4反应:Ba2++SO42-═BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +172.5KJ/mol | B. | -172.5KJ/mol | C. | -110.5KJ/mol | D. | -504 KJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用分液漏斗分离除去溴苯中混入的溴 | |
| B. | 顺-2-丁烯和反-2-丁烯的加氢产物不同 | |
| C. | 石油的裂解是化学变化,而石油的分馏和煤的干馏是物理变化 | |
| D. | 结构简式为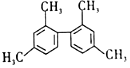 的分子中至少有11个碳原子处于同一平面上 的分子中至少有11个碳原子处于同一平面上 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从海水中可以得到 NaCl,电解饱和 NaCl 溶液可制备 Na | |
| B. | 锅炉水垢中含有的 CaSO4,可先用 Na2CO3溶液处理,后用酸除去 | |
| C. | 网络飞速发展,得益于光纤良好的导电性,光纤的主要成分是高纯度的单质硅 | |
| D. | 钢铁器件镀金既能增加美观,又能在镀层局部破损后防止器件损耗 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
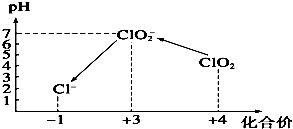 ClO2气体是一种常用的消毒剂,我国从2000年起逐步用ClO2代替氯气对饮用水进行消毒.
ClO2气体是一种常用的消毒剂,我国从2000年起逐步用ClO2代替氯气对饮用水进行消毒.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3溶液与盐酸:CO32-+2H+═H2O+CO2↑ | |
| B. | 硝酸银溶液与铜:Cu+Ag+═Cu2++Ag | |
| C. | 在稀氨水中通入过量CO2:NH3•H2O+CO2═NH4++CO32- | |
| D. | 用醋酸除水垢:2CH3COOH+CaCO3═Ca2++2CH3COO-+H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 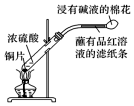 制取SO2并检验SO2的漂白性 | B. | 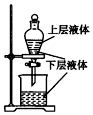 提取海带中的碘 | ||
| C. | 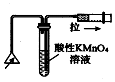 检验火柴燃烧产生的SO2 | D. | 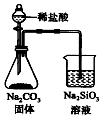 证明非金属性:Cl>C>Si |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质的沸点:W>Y | B. | 简单离子的半径:W>X | ||
| C. | 阴离子的还原性:Z<W | D. | Y与Z能形成离子化合物Y2Z2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com