
科目:高中化学 来源:2015-2016学年湖北省高一下学期期末化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A. 乙烷和乙烯均可使酸性KMnO4溶液褪色
B. 纤维素、淀粉和蛋白质都是高分子化合物
C. 煤的干馏和石油的分馏均属化学变化
D. 酯类和糖类均能发生水解反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一下学期期末化学试卷(解析版) 题型:选择题
下列反应属于取代反应的是 ( )
A.苯与溴水混合后振荡,水层褪色
B.乙烯通入酸性KMnO4溶液中,溶液褪色
C.CH4与Cl2的混合气体光照后颜色变浅
D.乙烯通入溴水中,溴水褪色
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西钦州市高二下学期期末化学B卷(解析版) 题型:简答题
下列物质都能发生水解反应,请说明水解的条件和生成物的类别:
(1)淀粉 (2)油脂 (3)蛋白质
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西钦州市高二下学期期末化学B卷(解析版) 题型:选择题
为扩大现有资源的使用效率,在一些油品中加入了降凝制剂J,以降低油料的凝固点,扩大燃料油的使用范围。J是一种高分子化合物:
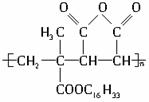
下列有关J的说法正确的是( )
A.J是由2种单体缩聚而成的
B.J是由2种单体加聚而成的
C.J具有可燃性
D.J没有可燃性
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省菏泽市高二联考化学试卷(解析版) 题型:实验题
用如图所示装置进行实验,将A逐滴加入B中:
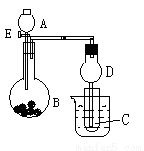
(1)若B为Na2CO3粉末,C为C6H5ONa溶液,实验中观察到小试管内溶液由澄清变浑浊,则试管C中化学反应的化学方程式: 。然后往烧杯中加入沸水,可观察到试管C中的现象: 。
(2)若B是生石灰,观察到C溶液中先形成沉淀,然后沉淀溶解。当沉淀完全溶解,恰好变澄清时,关闭E然后往小试管中加入少量乙醛溶液,再往烧杯中加入热水,静置片刻,观察到试管壁出现光亮的银镜,则A是 (填名称),C是 (填化学式),与乙醛的混合后,该溶液中反应的化学方程式: 。实验结束时用 清洗银镜。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省菏泽市高二联考化学试卷(解析版) 题型:选择题
下列说法中,正确的是
A.在紫外线、饱和(NH4)2SO4溶液、CuSO4溶液、福尔马林等作用下,蛋白质均会发生变性
B.在一定条件下,氨基酸之间能发生反应,合成更复杂的化合物(多肽)
C.为检验皂化反应进行程度,取几滴反应液,滴入装有热水的试管中,震荡,若有油滴浮在液面上,说明油脂已完全反应
D.检验淀粉在稀硫酸催化条件下水解产物的方法是:取适量水解液于试管中,加入少量新制Cu(OH)2悬浊液,加热煮沸,观察是否出现红色沉淀
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高二下学期期末化学试卷(解析版) 题型:填空题
锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的核外电子排布式为[Ar]____________,有__________个未成对电子。
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构角度分析,原因是________________。
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因_____________________。
GeCl4 | GeBr4 | GeI4 | |
熔点/℃ | ?49.5 | 26 | 146 |
沸点/℃ | 83.1 | 186 | 约400 |
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是______________。

(5)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为______________微粒之间存在的作用力是_____________。
(6)晶胞有两个基本要素:①原子坐标参数,表示晶胞内部各原子的相对位置,下图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为( ,0,
,0, );C为(
);C为( ,
, ,0)。则D原子的坐标参数为______。
,0)。则D原子的坐标参数为______。
②晶胞参数,描述晶胞的大小和形状,已知Ge单晶的晶胞参数a=565.76 pm,其密度为__________g·cm-3(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省雅安市高二下学期期末化学试卷(解析版) 题型:填空题
铬用于制不锈钢,汽车零件,工具,磁带和录像带等。铬是人体必需的微量元素,铬的生理功能是与其它控制代谢的物质一起配合起作用,如激素、胰岛素、各种酶类、细胞的基因物质(DNA和RNA)等,但铬在人体内超过一定浓度对人体健康会造成伤害。
(1)工业废水中常含有Cu2+等重金属离子,直接排放会造成污染,目前在工业废水处理过程中,依据沉淀转化的原理,常用FeS等难溶物质作为沉淀剂除去这些离子。已知室温下Ksp(FeS)=6.3×10-18,Ksp(CuS)=1.3×10-36。
请用离子方程式说明上述除杂的原理__________________。
(2)工业上为了处理含有Cr2O2- 7的酸性工业废水,用绿矾(FeSO4·7H2O)把废水中的六价铬离子还原成三价铬离子,再加入过量的石灰水,使铬离子转变为Cr(OH)3沉淀。
①氧化还原过程的离子方程式为__________。
②常温下,Cr(OH)3的溶度积Ksp=1×10-32,溶液的pH至少为 ,才能使Cr3+低于1×10-5 mol·L-1(国家允许的排放标准之内)。
③现用上述方法处理100m3含铬(+6价)78mg•L-1的废水,需用绿矾的质量为 kg。(保留到
小数点后一位)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com