
下列电子式书写正确的是
A.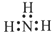 | B.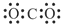 | C.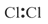 | D.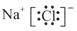 |
 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:单选题
用NA表示阿伏加德罗常数的值。下列叙述中不正确的是
| A.16.9 g过氧化钡(BaO2)固体中阴、阳离子总数约为0.2 NA |
| B.常温常压下,28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2 NA |
C.a g某气体含分子数为b,c g该气体在标况下的体积为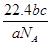 L L |
| D.某密闭容器盛有0.1 molN2和0.3 molH2,在一定条件下充分反应,转移电子的数目为0.6 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
设NA代表阿伏加德罗常数,下列叙述正确的是 ( )
| A.标准状况下2.24 L H2O中,分子数为0.1NA |
| B.将1mol Cl2通入到水中,则N(HClO)+ N(Cl?)+ N(ClO-)= 2NA |
| C.常温常压下16g O2和O3混合气体中,氧原子数为NA |
| D.7.8g Na2O2与足量水反应,转移电子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
设法把NO2和O2按4:1体积比充满一干燥的真空烧瓶中,然后把烧瓶置于水中,瓶内液面会逐渐上升,则最终烧瓶中所得溶液的物质的量浓度为(①气体体积为标准状况下测定 ②烧瓶中溶液不向外扩散)( )
| A.1/14mol/L | B.1/22.4mol/L | C.1/28mol/L | D.1/42mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
设NA代表阿伏加德罗常数的值,下列说法正确的是
| A.常温常压下22.4L SO2所含的分子数为NA |
| B.标准状况下22.4L CCl4所含的原子数为5NA |
| C.1L 1mol/L CaCl2溶液中所含的Cl-离子数为2NA |
| D.56 g Fe与任何物质完全反应时转移的电子数一定为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
设NA为阿伏加德罗常数的数值,下列叙述中正确的是
| A.常温常压下,100g8.5%的H2O2水溶液中含氧原子总数为NA |
| B.标准状况下,NA个H2O分子所占的休积为22.4L |
| C.标准状况下,2.24L乙烯分子中σ键为0.1NA |
| D.常温常压下,4.8g臭氧与4.8g氧气所含的氧原子数均为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
今有一包铁粉和铜粉混合粉末,为确定其组成,现提供4 mol·L-1的FeCl3溶液(其它用品略),某合作学习小组同学的实验结果如下(假定反应前后溶液体积不变):
| 组别 | ① | ② | ③ | ④ |
| V[FeCl3(aq)]/mL | 100 | 100 | 100 | 100 |
| 混合粉末质量/g | 6 | 13.2 | 24 | 36 |
| 反应后剩余固体质量/g | 0 | 1.28 | 12.8 | 24.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com