
【题目】已知甲苯可以进行如下转化:

回答下列问题:
(1)反应①的反应类型为__________,反应③的反应类型为_____________。
(2)化合物A的结构简式为____________。化合物D的分子式为_____________。
(3)反应②的化学方程式为_______________________________。
科目:高中化学 来源: 题型:
【题目】在FeBr2和FeI2混合溶液中逐渐通入氯气,不可能发生的反应离子方程式是( )
A. 2I-+Cl2===I2+2Cl-
B. 2Fe2++2Br-+2I-+3Cl2===2Fe3++I2+Br2+6Cl-
C. 2Fe2++4Br-+2I-+4Cl2===2Fe3++I2+2Br2+8Cl-
D. 4Fe2++2Br-+2I-+4Cl2===4Fe3++I2+Br2+8Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )

A. 由 图甲可知,a点Kw的数值比b点Kw的数值大
B. 乙表示在相同的密闭容器中,不同温度下的反应,该反应的ΔH<0
C. 丙表示0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.100 0 mol·L-1醋酸溶液的滴定曲线
D. 根据图丁,除去CuSO4溶液中的Fe3+,可加入CuO调节pH至3~5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铝粉和四氧化三铁粉末配成铝热剂,分成两等份:一份在高温下恰好反应,再与足量稀硫酸反应, 生成氢气aL;另一份直接放入足量氢氧化钠溶液中充分反应,在同条件下生成氢气bL,则a∶b为( )
A. 1∶1 B. 3∶4 C. 4∶3 D. 8∶9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢铁中含有C、N、Mn等元素,实验中常用过硫酸盐氧化法测定钢铁中锰的含量,反应原理为2Mn2++5S2O82-+8H2O![]() 2MnO4-+10SO42-+16H+
2MnO4-+10SO42-+16H+
(1)Mn原子的价层电子的轨道衷达式(电子排布图)为______。
(2)已知H2S2O8的结构简式如图所示。
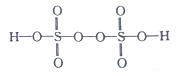
①H2S2O8中S的轨道杂化方式为______,H、O、S三种元素中,电负性最大的元素是_________(填元素符号)。
②S基态原子中电子的运动状态有_________种。
③上述反应中S2O82-断裂的共价键类型为________,(填“σ键”或“π键”) ,每生成1molMnO4-,断裂的共价键数目为_________NA。
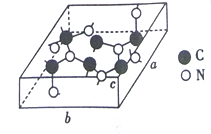
(3)C和N能形成多种结构的晶体。一种新型的超硬材料类似于金刚石的结构,但硬度比金刚石大,其晶胞如图所示(图示原子都包含在晶胞内),其化学式为________。已知晶胞参数a=0.64nm, b=0.55nm,c=0.24nm,则该晶体的密度为________(列出式子即可,但式子中不包含字母)g/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1,2-二氯乙烷常温下为无色液体,沸点为83.5 ℃,密度为1.23 g·mL-1,难溶于水,易溶于醇、醚、丙酮等有机溶剂。乙醇的沸点为78.5 ℃。某化学课外活动小组为探究1,2-二氯乙烷的消去反应,设计了如下图所示的实验装置。

请回答下列问题。
(1)为了检验整套装置的气密性,某同学将导气管末端插入盛水的烧杯中,用双手捂着装置A中大试管,但几乎不能说明装置是否密闭。请回答如何检查装置气密性:____________。
(2)向装置A中大试管里先加入1,2-二氯乙烷和NaOH的乙醇溶液,再加入___________,目的是______________________________,并向装置C中试管里加入适量稀溴水。
(3)与装置A中大试管相连接的长玻璃管的作用是 ____________________________,装置B的作用是 ______________________________________________。
(4)证明1,2-二氯乙烷已发生消去反应的现象是_________________________________,装置A、C中发生反应的化学方程式分别为:___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某气体反应的平衡常数可表示为K=c(CH3OCH3)c(H2O)/c2(CH3OH),该反应在不同温度下的平衡常数:400℃,K=32;500℃,K=44。请回答下列问题:
(1)写出上述反应的化学方程式:_________________________________ 。
(2)该反应的△H _________0。
(3)已知在密闭容器中,测得某时刻各组分的浓度如下:
物质 | CH3OH(g) | CH3OCH3(g) | H2O(g) |
浓度/(molL-1) | 0.54 | 0.68 | 0.68 |
①此时温度400℃,则某时刻υ正_______υ逆(填<、>或=,下同)。
②若以温度为横坐标,以该温度下平衡态甲醇物质的量n为纵坐标,此时反应点在图象的位置是图中____点,比较图中B、D两点所对应的正反应速率υB_______υD,理由是____。

(4)一定条件下要提高反应物的转化率,可以采用的措施是___________。
a.升高温度 b.加入催化剂 c.压缩容器的体积
d.增加水蒸气的浓度 e.及时分离出产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.有下列物质:①Fe ②NH4Cl溶液③Na2O ④Cu(OH)2 ⑤熔融的MgCl2 ⑥H2SO4 ⑦CO2 ⑧C2H5OH(酒精)(用序号作答)。其中属于电解质的有_____________,属于非电解质的有________________。
Ⅱ、某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+、Fe3+、Na+中的几种,请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是________。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子所发生的离子方程式为______________________________________。
(3)取(2)中的滤液,加入过量的NaOH出现白色沉淀,说明原溶液中肯定有的该离子所发生的离子方程式为___________________________。
(4)通过以上实验确定原溶液中一定含有的阳离子是_________,不能确定的阳离子是_________。
(5)原溶液可能大量存在的阴离子是下列的________。
A.Cl- B.NO![]() C.CO
C.CO![]() D.OH-
D.OH-
Ⅲ.现有M、N两种气态化合物,其摩尔质量之比为2:1,试回答下列问题:
(1)同温同压下,M、N气体的密度之比为____________。
(2)相同温度下,在两个相同体积的密闭容器中分别充入M、N,若两个容器中气体的密度相等,则两个容器中的压强之比为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com