
����Ŀ��ij����С���ͬѧ����ʵ������п��Ũ���ᷴӦ��ʵ���У���ͬѧ��Ϊ�����������Ƕ���������ͬѧ��Ϊ���������������⣬�����ܲ���������Ϊ����֤��λͬѧ���ж���ȷ����ͬѧ�������ͼ1��ʾʵ��װ�ã�п��Ũ���Ṳ��ʱ����������ΪX�����巢��װ����ȥ�����Իش� 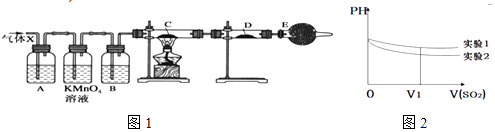
��1��������Ӧ�����ɶ�������Ļ�ѧ����ʽΪ ��
��2����ͬѧ��Ϊ�����ܲ��������������� ��
��3��A�м�����Լ������� �� ��������B�м�����Լ������� �� ��������
��4������֤������X�к���������ʵ�������ǣ�C�У� �� D�У� ��
��5��II����С��ͬѧ���ռ���SO2����ͨ��0.1molL��1��Ba��NO3��2��Һ�У��õ���BaSO4������Ϊ̽��������Һ�к�����������ͨ���SO2 �� ��С����������¼��裺 ����һ����Һ�е�NO3��
���������Һ���ܽ��O2
��С�����ʵ����֤�˼���һ��
�����±��հ״���д���ʵ������
ʵ�鲽�� | ʵ������ | ���� |
ʵ��1����ʢ�в���O2��25ml0.1mol/LBaCl2��Һ���ձ��У�����ͨ�봿����SO2���� | ����һ���� | |
ʵ��2����ʢ�в���O2��25ml0.1mol/LBa��NO3��2��Һ���ձ��У�����ͨ�봿����SO2���� |
��6��Ϊ�����о��÷�Ӧ����С�黹�����������ʵ������Һ��pH��ͨ��SO2����ı仯������ͼ2��ʵ��1����ҺpH��С��ԭ����V1ʱ��ʵ��2����ҺpHС��ʵ��1��ԭ���ǣ������ӷ���ʽ��ʾ�� ��
���𰸡�
��1��Zn+2H2SO4��Ũ�� ![]() ?ZnSO4+SO2��+2H2O
?ZnSO4+SO2��+2H2O
��2����Zn��ŨH2SO4��Ӧ�����У�H2SO4����������ˮ���ɣ�H2SO4Ũ����С�����ϡ���ᣬZn��ϡH2SO4��Ӧ����H2
��3��Ʒ����Һ������SO2��ŨH2SO4������ˮ����
��4����ɫ��CuO����ĩ��ɺ�ɫ��Cu������ɫ��ĩ�����ɫ
��5��������ɫ��������
��6��SO2����ˮ������H2SO3 �� �����������ԣ���pHֵ��С��3SO2+2H2O+2NO3�� ![]() ?2NO+4H++3SO42����
?2NO+4H++3SO42����
���������⣺��1������������п��Ũ���ᷴӦ�õ���п��Ũ���ᷴӦ�ö�����������п��ˮ����Ӧ�Ļ�ѧ����ʽΪ��Zn+2H2SO4��Ũ�� ![]() ZnSO4+SO2��+2H2O�� ���Դ��ǣ�Zn+2H2SO4��Ũ��
ZnSO4+SO2��+2H2O�� ���Դ��ǣ�Zn+2H2SO4��Ũ�� ![]() ZnSO4+SO2��+2H2O����2����Zn��ŨH2SO4��Ӧ�����У�H2SO4����������ˮ���ɣ�H2SO4Ũ����С�����ϡ���ᣬZn��ϡH2SO4��Ӧ����H2��
ZnSO4+SO2��+2H2O����2����Zn��ŨH2SO4��Ӧ�����У�H2SO4����������ˮ���ɣ�H2SO4Ũ����С�����ϡ���ᣬZn��ϡH2SO4��Ӧ����H2��
���Դ��ǣ���Zn��ŨH2SO4��Ӧ�����У�H2SO4����������ˮ���ɣ�H2SO4Ũ����С�����ϡ���ᣬZn��ϡH2SO4��Ӧ����H2�� ��3������װ��ͼ��֪�����ɵ��������ж������������������װ��A����֤����������ڵ�װ�ã�ѡƷ����Һ������֤��ͨ�����������Һ��ȥ��������ͨ��װ��B�е�Ũ�����ȥˮ������
���Դ��ǣ�Ʒ����Һ������SO2��ŨH2SO4������ˮ��������4��֤�����ɵ������к���ˮ����������Cװ���к�ɫ����ͭ��Ϊ��ɫͭ��Dװ���а�ɫ����ͭ��Ϊ��ɫ��
���Դ��ǣ���ɫ������ͭ����ĩ��ɺ�ɫ��ͭ������ɫ��ĩ�����ɫ����5������������Դ��������ᣬ������������Ȼ�������Ӧ����ʵ��1��������
Ba��NO3��2��Һ�л���ͨ�봿����SO2���壬����������ԭ��Ӧ�������ᱵ��������ʵ��2�����ɰ�ɫ����������һ������
���Դ��ǣ�
ʵ�鲽�� | ʵ������ | ���� |
ʵ��1����ʢ�в���O2��25mL0.1molL��1BaCl2��Һ���ձ��У�����ͨ�봿����SO2���� | ������ | ����һ���� |
ʵ��2����ʢ�в���O2��25mL0.1molL��1Ba��NO3��2��Һ���ձ��У�����ͨ�봿����SO2���� | ��ɫ�������� |
;��6��ʵ��1����ҺpH��С��ԭ����SO2����ˮ������H2SO3 �� �����������ԣ���pHֵ��С��ʵ��2����ҺpHС��ʵ��1��ԭ����3SO2+2H2O+2NO3��=2NO+4H++3SO42�� ��
���Դ��ǣ�SO2����ˮ������H2SO3 �� �����������ԣ���pHֵ��С��3SO2+2H2O+2NO3�� ![]() 2NO+4H++3SO42�� ��
2NO+4H++3SO42�� ��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ҫ��ȥ�Ȼ�����Һ�к��е�����̼���ƣ��ɲ��õķ����ǣ� ��
A.ͨ��������CO2B.���������BaCl2��Һ
C.����������ϡ����D.���������ϡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ��þʯ(��Ҫ�ɷ�ΪMgCl2��6H2O)Ϊԭ��������ʽ̼��þ����Ҫ�������£�
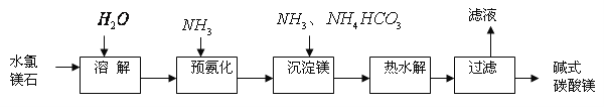
��1�����������е���ҺŨ���ᾧ��������Ҫ�������ʵĻ�ѧʽΪ___________________���������������ӵ�ʵ�鷽����__________________________________________________��
��2�����������еĹ��˲������õ���Ҫ����������________________________________��
��3���������ռ�ʽ̼��þ�õ�MgO��ȡ��ʽ̼��þ4.66g���������������أ��õ�����2.00g�ͱ�״����CO2 0.896L��ͨ������ȷ����ʽ̼��þ�Ļ�ѧʽ_____(д��������̣����÷�)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����4 g NaOH�����ܽ���ˮ����1 L��Һ������ȡ��10 mL����10 mL��Һ�����ʵ���Ũ����(����)
A. 1 mol��L-1 B. 0.1 mol��L-1 C. 0.01 mol��L-1 D. 10 mol��L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧϰ��ȤС�������ø�����������Ҫ�ɷ���Al2O32SiO22H2O���Ʊ����͵ľ�ˮ����ʵ��������ͼ�� 
������ҺC�������Ʊ��ľ�ˮ����������������⣺
��1�������A��B����ҺC������D����Ҫ�ɷ֣�A��B��CD ��
��2��д���������봿��������ڵ�������ѧ����ʽ����
��3����ʵ���У����ڸ�����������Ļ�������ѡ�õ������� ��
A.��������
B.������
C.����������
D.��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. ����ʱ�軯ѧ���ʲ����ã��������κ����ʷ�Ӧ
B. �������н��������Ե��磬���ڽ�������
C. Na2SiO3���Ʊ��轺��ľ�ķ������ԭ��
D. ���������ǽ�̫����ת��Ϊ���ܵij��ò���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������ȼ���ұ�����۽�����ԭ����
A. ���ĵ����Ժܺ�
B. �ڸ�������ȼ��
C. ��ԭ�Խ�ǿ���ڷ�Ӧ�зų���������
D. ���ڿ��������ȶ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������������´ɡ��մɡ������������ϵ���ɫ�����ɸ�̼�����Ͻ𣨺�Cr��Fe��C���Ʊ������������Ĺ����������£�
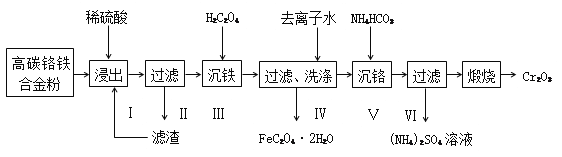
��֪��Cr(OH)3���������������������Ϊ���
�ش��������⣺
��1����������ȡʱ��Ϊ��߽�ȡ���ʣ�������̼�����Ͻ��Ƴɷ�ĩ�⣬���ɲ�ȡ�Ĵ�ʩ��__________________________��дһ�㣩����ȡ��ʱ��Ӧ�����ӷ���ʽΪ_______________��
��2�����������������ٴν�ȡ��Ŀ����_____________________________________________��
��3������������ʱ����Һ��pH������ȥ����Ӱ����ͼ1��ʾ��

ͼ1 ͼ2
pHС��2.3ʱ����ȥ���ʵͣ���ԭ����_______________________________________��
��4����������˵��������ϴ�Ӹɾ��IJ�����________________________________________��
��5������������ʱ������Cr(OH)3�Ļ�ѧ����ʽΪ_____________________________������ʱ����ҺpH����Ļ����ʹ�ϵ��ͼ2��ʾ����pH��8.5ʱ��pHԽ���Ļ�����Խ�ͣ������ԭ����____________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2016��ŵ������ѧ���ɷ���Ӣ����������ѧ�ҷֻ��Ա��������ڷ��ӻ����о�����ijɾ͡�����ϩ�Ƿ��ӻ����ij����м��壬��ϳɷ������£�

�� �� ��
����˵����ȷ����
A. ������������������Ϊ�� B. ����ϩһ��ȡ������3��
C. �����������ɻ�������Ϊȡ����Ӧ D. ��Ȳ�뱽��Ϊͬ���칹��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com