
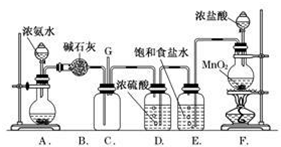
分析 (1)实验室用二氧化锰和浓盐酸反应制备氯气,二者在加热条件下反应生成氯气、氯化锰和水;
(2)浓盐酸具有挥发性,加热能够促进盐酸的挥发制取的氯气中含有氯化氢气体,依据氯气、氯化氢溶解性解答;
(3)C内出现浓厚的白烟为氯化铵,另一生成物是空气的主要成分之一为氮气,据此写出方程式;
(4)根据氯气能够与氢氧化钠溶于反应的性质来确定尾气处理的方法.
解答 解:(1)二氧化锰和浓盐酸在加热条件下反应生成氯气、氯化锰和水,离子方程式:MnO2+4H++2C1-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++C12↑+2H2O;
故答案为:MnO2+4H++2C1-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++C12↑+2H2O;
(2)浓盐酸具有挥发性,加热能够促进盐酸的挥发制取的氯气中含有氯化氢气体,氯气在饱和食盐水中溶解度不大,氯化氢极易溶于水,所以E装置中盛放的饱和食盐水,用来除去氯气中混有的氯化氢气体;
故答案为:除去氯气中混有的氯化氢气体;
(3)C内出现浓厚的白烟为氯化铵,另一生成物是空气的主要成分之一为氮气,该反应为3Cl2+8NH3═N2+6NH4Cl,
故答案为:3Cl2+8NH3═N2+6NH4Cl;
(4)氯气是酸性气体,能够与氢氧化钠反应生成氯化钠、次氯酸钠和水,所以可以用氢氧化钠来进行尾气处理,或者是通入装有碱石灰的干燥管或气球收集,G处接NaOH溶液的尾气处理装置;
故答案为:G处接NaOH溶液的尾气处理装置.
点评 本题考查学生实验室制取氯气、氨气的方法、干燥、性质等,熟悉氨气的制取、氯气的制取原理及物质的性质是解答本题的关键,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A1Cl3、NH3•H20 | B. | ZnCl2、NH3•H20 | C. | A1Cl3、NaOH | D. | ZnCl2、NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某有机物结构如图,它不可能具有的性质是( )
某有机物结构如图,它不可能具有的性质是( )| A. | ①⑤⑦ | B. | ①②③④⑥⑦ | C. | ⑤⑦ | D. | ⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com