
| A、油脂的皂化反应 |
| B、在光照条件下,甲烷与氯气的反应 |
| C、酯化反应 |
| D、乙烯通入溴的四氯化碳溶液中的反应 |


科目:高中化学 来源: 题型:
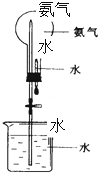 哈伯因为氨气的合成曾获1918年诺贝尔奖.
哈伯因为氨气的合成曾获1918年诺贝尔奖.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、ICl3与水反应的产物为HI和HClO |
| B、ICl3与KI反应时,氯元素被还原 |
| C、ICl与冷NaOH溶液反应的离子方程式为:ICl+2OH-=IO-+Cl-+H2O |
| D、ICl与水的反应属于氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HN3水溶液中微粒浓度大小顺序为:c(HN3)>c(H+)>c(N3-)>c(OH-) |
| B、题示500mL溶液中离子浓度大小顺序为:c(Na+)>c(N3-)>c(OH-)>c(H+) |
| C、题示500mL溶液中由水电离产生的c(OH-)=1×10-αmol?L-1 |
| D、根据题给出的数据可以计算该温度喜爱叠氮酸的电离平衡常数Kα |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=5的H2S溶液中,c(H+)=c(HS-)=1×10-5 mol/L |
| B、pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1 |
| C、pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+c(H+)=c(OH-)+c(HC2O4-) |
| D、pH相同的①CH3COONa、②NaHCO3两种溶液的c(Na+):①>② |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 200 | 300 | 400 |
| K | 1.0 | 0.68 | 0.5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com