
| A. | 6.02×1023个N2 | B. | 9g H2O | C. | 0.5mol Br2 | D. | 10g H2 |
科目:高中化学 来源: 题型:选择题
| 选项 | 陈述I | 陈述Ⅱ |
| A | 苯不能使酸性高锰酸钾溶液褪色;甲苯能使酸性高锰酸钾溶液褪色. | 甲基使苯环性质变活泼 |
| B | 与浓硫酸、浓硝酸混合物发生一元硝化反应时,苯需60℃,而甲苯只需30℃ | 苯环使甲基性质变活泼 |
| C | CH2=C(CH3)CH=CH2和Br2在一定条件下物质的量1:1发生加成反应,可生成3种有机物. | CH2=C(CH3)CH=CH2可发生1,2加成和1,4加成. |
| D | 卤代烷中加入NaOH乙醇共热,冷却后滴入AgNO3溶液,则有白色沉淀生成 | 卤代烷是氯代烷 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2AgNO3+MgCl2═2AgCl↓+Mg(NO3)2 | B. | K2CO3+Ca(OH)2═CaCO3↓+2KOH | ||
| C. | CaCl2+CO2+H2O═CaCO3↓+2HCl | D. | HCl+KOH═KCl+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
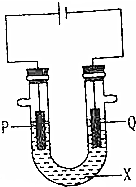 为探究工业生产氯气的原理,某同学设计了如图的实验装置,其中U型管中装有物质X,并乙滴入几滴酚酞试液,P,Q两根石墨棒作为电极,通过导线与直流电源相连.请回答以下问题.
为探究工业生产氯气的原理,某同学设计了如图的实验装置,其中U型管中装有物质X,并乙滴入几滴酚酞试液,P,Q两根石墨棒作为电极,通过导线与直流电源相连.请回答以下问题.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氮磷砷锑铋位于周期表第ⅤA族,它们的单质及其化合物在社会生产生活中有广泛应用,请回答有关问题:
氮磷砷锑铋位于周期表第ⅤA族,它们的单质及其化合物在社会生产生活中有广泛应用,请回答有关问题: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 乙醇在一定的条件下发生化学反应时,化学键断裂的情况如图所示.当乙醇和氧气发生催化氧化时,化学键断裂的位置是 ( )
乙醇在一定的条件下发生化学反应时,化学键断裂的情况如图所示.当乙醇和氧气发生催化氧化时,化学键断裂的位置是 ( )| A. | 2 3 | B. | 2 4 | C. | 1 3 | D. | 3 4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com