
【题目】已知阿伏加德罗常数的值为NA。下列说法正确的是( )
A. 标准状况下,2.24LCCl4含有的共价键数为0.4NA
B. 常温下,14 g的![]() 含中子数目为6NA
含中子数目为6NA
C. 用铂电极电解100 mL 1 mol L-1的CuSO4溶液足够长时间,转移电子数一定为0.2NA
D. 将含3NA个离子的Na2O2固体溶于水配成1L溶液,所得溶液中Na+的浓度为2mol/L
【答案】D
【解析】
A.在标准状况下,CCl4是液态,不能使用气体摩尔体积,A错误;
B. 14 g![]() 的物质的量是1mol,1个
的物质的量是1mol,1个![]() 原子中含有8个中子,所以1mol
原子中含有8个中子,所以1mol![]() 中含有中子数目为8NA,B错误;
中含有中子数目为8NA,B错误;
C. 100 mL 1 mol L-1的CuSO4溶液中含有溶质的物质的量是n(CuSO4)=1mol/L×0.1L=0.1mol。用铂电极电解100 mL 1 mol L-1的CuSO4溶液,开始时,溶液中Cu2+放点,产生Cu单质,当Cu2+放电完全后,溶液中的H+放电,产生H2,因此电解足够长时间,转移电子数大于0.2NA,C错误;
D.含3NA个离子的Na2O2固体中,Na2O2的物质的量是1mol,溶于水反应产生2molNaOH,由于溶液的体积是1L,所以Na+的物质的量浓度c(Na+)=2mol÷1L=2mol/L,D正确。
故本题合理选项是D。


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源: 题型:
【题目】在体积为2L的恒容密闭容器中充入一定量的SO2和O2,发生反应:2SO2(g)+O2(g) ![]() 2SO3(g)反应在三种不同的条件下进行,反应物SO2的物质的量(mol)随反应时间(min)的变化情况如下表所示:
2SO3(g)反应在三种不同的条件下进行,反应物SO2的物质的量(mol)随反应时间(min)的变化情况如下表所示:
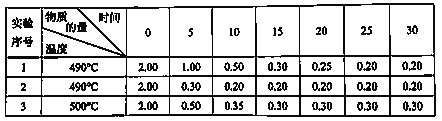
(1)对照实验1,实验2改变的某一外界条件可能是_______。
(2)反应达平衡后,向实验2中加入少量的18O2,一段时间18O后可能存在于哪些物质中________(填选项)。
A 只存在氧气 B 只存在三氧化硫 C 只存在反应物 D 存在反应物与生成物
(3)实验3中,在5~15min时段,用O2表示的平均反应速率为______ mol/(L·min)。
(4)若将实验1置于绝热体系中,测得实验到达平衡的时间比原来缩短了,则参加反应的SO2和O2的总能量______(填“>”、“<”或“=”)生成的SO3的总能量。
(5)能说明实验3达到平衡状态的标志是_______(任写一条)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为周期表的一部分,其中的编号代表对应的元素。
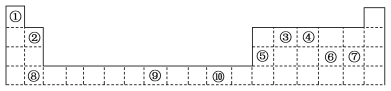
请回答下列问题:
(1)表中属于d区的元素是________(元素符号)。
(2)写出元素溴的基态原子的简化电子排布式_____________________,写出⑩的价电子排布图_____________________________________。
(3)某元素⑦的原子核外最外层电子的成对电子为________对。
(4)元素④的氢化物的分子构型为________,中心原子的杂化形式为________。
(5)第三周期8种元素按单质熔点高低的顺序如下图,其中序号“⑧”为________(填元素符号);其中电负性最大的是________(填元素符号)。
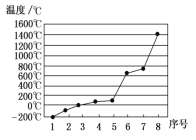
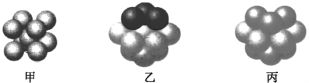
(6)⑩的基态原子有____种能量不同的电子;如图___(填“甲”、“乙”或“丙”)表示的是⑩晶体中微粒的堆积方式。晶体中距离一个⑩原子最近的⑩原子有____个。若该晶体中一个晶胞的边长为a pm,则⑩晶体的密度为__________g.cm-3(写出含a的表达式,用NA表示阿伏加德罗常数的值,不需化简)。若⑩的原子半径为r,则⑩晶胞这种堆积模型的空间利用率为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】皂化反应实验的操作步骤如下:
①在小烧杯中加入约5 g 新鲜的动物脂肪(如牛油)和6 mL 95%的乙醇,微热使脂肪完全溶解;
②在①的混合液中加入6 mL 40%的氢氧化钠溶液,边搅拌边加热,直至反应液变成黄棕色黏稠状;
③用玻璃棒蘸取反应液,滴入装有热水的试管中,振荡,若无油滴浮在液面上,说明反应液中油脂已完全反应,否则要继续加热使之反应完全;
④在另一只烧杯中加入60 mL 热的饱和食盐水,把得到的反应液倒入食盐水中,搅拌,观察浮在液面上的固体物质,取出,用滤纸或纱布吸干,挤压成块,并与日常使用的肥皂比较去污能力的大小。
根据上面的实验步骤,请回答下列问题:
(1)加入乙醇的原因是_______________________________________。
(2)请写出硬脂酸甘油酯发生皂化反应的化学方程式:__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知α氨基酸在一定条件下能与亚硝酸(HNO2)反应得到α羟基酸。如:![]() +N2↑+H2O,试根据下图所示关系回答下列有关问题。
+N2↑+H2O,试根据下图所示关系回答下列有关问题。
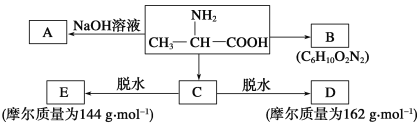
(1)写出A、B的结构简式:
A________________________________________________________________________;
B________________________________________________________________________。
(2)写出C→D的化学方程式:________________________________________。
(3)写出C→E的化学方程式:___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子中的离子,能在溶液中大量共存的是( )
A.Na+、K+、SO42- 、NO3-B.K+、Ca2+、CO32- 、NO3-
C.Na+、NH4+、Cl- 、OH-D.Na+、H+ 、OH- 、Mg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数之和为46,它们在周期表中的相对位置如图所示。下列说法正确的是
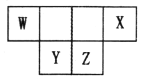
A. 原子半径大小顺序为:Y>Z>X
B. X元素最高价氧化物的水化物酸性最强
C. Y元素的简单氢化物稳定性最强
D. Z单质难溶于化合物WZ2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的密闭容器中,加入1 mol CO和1 mol H2O,发生反应:CO(g)+H2O(g)![]() CO2(g)+H2(g),达到平衡时测得n(H2)为0.5 mol,下列说法不正确的是( )
CO2(g)+H2(g),达到平衡时测得n(H2)为0.5 mol,下列说法不正确的是( )
A. 在该温度下平衡常数K=1
B. 平衡常数与反应温度无关
C. CO的转化率为50%
D. 其他条件不变改变压强平衡不移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。已知![]() ,若以乙烯为主要原料合成乙酸,其合成路线如图所示:
,若以乙烯为主要原料合成乙酸,其合成路线如图所示:
![]()
反应②的化学方程式为_____________________________,反应类型是_______。工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物,其反应的化学方程式为_______________________________,反应类型是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com