
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®ÓŠŠ©»īĘĆ½šŹōČēĀĮæÉ×÷»¹Ō¼Į·ØµÄ»¹Ō¼Į
B£®ÓƵē½āNaClČÜŅŗµÄ·½·ØĄ“Ņ±Į¶½šŹōÄĘ
C£®æÉÓĆ½¹Ģæ»ņŅ»Ńõ»ÆĢ¼»¹ŌŃõ»ÆĀĮµÄ·½·ØĄ“Ņ±Į¶ĀĮ
D£®»ŲŹÕ¾É½šŹōæÉŅŌÖŲŠĀÖĘ³É½šŹō»ņĖüĆĒµÄ»ÆŗĻĪļ
 ÄĻ“ó½ĢøØĒĄĻČĘšÅÜŹī¼ŁĻĪ½Ó½Ģ³ĢÄĻ¾©“óѧ³ö°ęÉēĻµĮŠ“š°ø
ÄĻ“ó½ĢøØĒĄĻČĘšÅÜŹī¼ŁĻĪ½Ó½Ģ³ĢÄĻ¾©“óѧ³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğø£½ØŹ”ø߶žĻĀŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŹµŃéĢā
ÓĆĮāĆĢæó£ØÖ÷ŅŖŗ¬MnCO3”¢FeCO3”¢Al2O3”¢SiO2£©ÖʱøMnSO4”¤H2OµÄ¹¤ŅÕĮ÷³ĢČēĻĀ£ŗ
¢ń£®ĻņĮāĆĢæóÖŠ¼ÓČė¹żĮæĻ”H2SO4£¬¹żĀĖ£»
¢ņ£®ĻņĀĖŅŗÖŠ¼ÓČė¹żĮæMnO2£¬¹żĀĖ£»
¢ó£®µ÷½ŚĀĖŅŗpH=a£¬¹żĀĖ£»
¢ō£®ÅØĖõ”¢½į¾§”¢·ÖĄė”¢øÉŌļµĆµ½²śĘ·£»
¢õ£®¼ģŃé²śĘ·“æ¶Č”£
£Ø1£©²½Öč¢ńÖŠ£¬ĀĖŌüµÄÖ÷ŅŖ³É·ÖŹĒ ”£
£Ø2£©½«MnO2Ńõ»ÆFe2+µÄĄė×Ó·½³ĢŹ½²¹³äĶźÕū£ŗ
 MnO2 +
MnO2 + Fe2++
Fe2++ £½
£½ Mn2+ +
Mn2+ +  Fe3+ +
Fe3+ +
£Ø3£©ÓėŃ”ÓĆCl2×÷ĪŖŃõ»Æ¼ĮĻą±Č£¬MnO2µÄÓÅŹĘÖ÷ŅŖŌŚÓŚ£ŗŌĮĻĄ“Ō“¹ć”¢³É±¾µĶ”¢æɱÜĆā»·¾³ĪŪČ¾”¢ ”£
£Ø4£©ŅŃÖŖ£ŗÉś³ÉĒāŃõ»ÆĪļ³ĮµķµÄpH
Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 | |
æŖŹ¼³ĮµķŹ± | 3.4 | 6.3 | 1.5 | 7.6 |
ĶźČ«³ĮµķŹ± | 4.7 | 8.3 | 2.8 | 10.2 |
×¢£ŗ½šŹōĄė×ÓµÄĘšŹ¼ÅضČĪŖ0.1mol/L
²½Öč¢óÖŠaµÄȔֵ·¶Ī§ŹĒ ”£
£Ø5£©²½Öč¢õ£¬Ķعż²ā¶Ø²śĘ·ÖŠĆĢŌŖĖŲµÄÖŹĮæ·ÖŹżĄ“ÅŠ¶Ļ²śĘ·“æ¶Č”£
ŅŃÖŖŅ»¶ØĢõ¼žĻĀ£¬MnO4£ÓėMn2+·“Ӧɜ³ÉMnO2 ”£Č”x g²śĘ·Åä³ÉČÜŅŗ£¬ÓĆ0.1mol/L KMnO4ČÜŅŗµĪ¶Ø£¬ĻūŗÄKMnO4ČÜŅŗy mL£¬²śĘ·ÖŠĆĢŌŖĖŲµÄÖŹĮæ·ÖŹżĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğÖŲĒģĖÄŹ®¶žÖŠøßŅ»ĻĀĘŚÖŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŅŃÖŖ¼øÖÖ¶ĢÖÜĘŚŌŖĖŲµÄŌ×Ó°ė¾¶”¢³£¼ūµÄ×īøß¼ŪŗĶ×īµĶ¼ŪČēĻĀ±ķ£¬ĻĀĮŠĖµ·ØĻĀ²»ÕżČ·µÄŹĒ£Ø £©
ŌŖĖŲŠŌÖŹ | ŌŖĖŲ±ąŗÅ | ||||||
¢Ł | ¢Ś | ¢Ū | ¢Ü | ¢Ż | ¢Ž | ¢ß | |
Ō×Ó°ė¾¶£Ønm£© | 0.073 | 0.075 | 0.152 | 0.110 | 0.099 | 0.186 | 0.143 |
×īøßÕż»ÆŗĻ¼Ū | ĪŽ | +5 | +1 | +5 | +7 | +1 | +3 |
×īµĶøŗ»ÆŗĻ¼Ū | ©2 | ©3 | ĪŽ | ©3 | ©1 | ĪŽ | ĪŽ |
A£®¢ßµÄ¼ņµ„Ąė×Ó²»ŹĒĶ¬ÖÜĘŚŌŖĖŲĄė×Ó°ė¾¶×īŠ”µÄ
B£®ĘųĢ¬Ēā»ÆĪļµÄĪČ¶ØŠŌ¢Ł£¾¢Ś
C£®¢ŚµÄĘųĢ¬Ēā»ÆĪļÅØČÜŅŗæÉÓĆÓŚ¼ģŃéĀČĘų¹ÜµĄµÄŠ¹Ā©
D£®ŅõĄė×ӵĻ¹ŌŠŌ¢Ü“óÓŚ¢Ż£¬×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļµÄ¼īŠŌ¢ŪŠ”ÓŚ¢Ž
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğÖŲĒģĖÄŹ®¶žÖŠøßŅ»ĻĀĘŚÖŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŌŖĖŲŠŌÖŹ³ŹÖÜĘŚŠŌ±ä»ÆµÄ¾ö¶ØŅņĖŲŹĒ£Ø £©
A. ŌŖĖŲŌ×Ó°ė¾¶“󊔳ŹÖÜĘŚŠŌ±ä»Æ
B. ŌŖĖŲĻą¶ŌŌ×ÓÖŹĮæŅĄ“ĪµŻŌö
C. ŌŖĖŲŌ×Ó×īĶā²ćµē×ÓÅŲ¼³ŹÖÜĘŚŠŌ±ä»Æ
D. ŌŖĖŲµÄ×īøßÕż»ÆŗĻ¼Ū³ŹÖÜĘŚŠŌ±ä»Æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğŗ£ÄĻŹ”øßŅ»ĻĀŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
£Ø1£©µŚČżÖÜĘŚŌŖĖŲÖŠ£¬»ÆѧŠŌÖŹ×ī²»»īĘƵďĒ £¬æÉÓĆÓŚÖĘ°ėµ¼Ģå²ÄĮĻµÄŌŖĖŲŹĒ_______.
£Ø2£©ClŌŖĖŲŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆŹĒ ÖÜĘŚ ×唣
£Ø3£©µŚČżÖÜĘŚŌŖĖŲÖŠŌŖĖŲÖŠ£¬×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļ¼īŠŌ×īĒæµÄŹĒ £¬ĖįŠŌ×īĒæµÄŹĒ £¬³ŹĮ½ŠŌµÄŹĒ £»
£Ø4£©ŌŚC”¢N”¢O”¢FÖŠ£¬Ō×Ó°ė¾¶×ī“óµÄŹĒ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğŗ£ÄĻŹ”øßŅ»ĻĀŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŅŌĻĀ¹ŲÓŚ¼×ĶéµÄĖµ·ØÖŠ“ķĪóµÄŹĒ
A£®¼×Ķé·Ö×Ó¾ßÓŠÕżĖÄĆęĢå½į¹¹
B£®¼×Ķé»ÆѧŠŌÖŹ±Č½ĻĪČ¶Ø£¬²»±»ČĪŗĪŃõ»Æ¼ĮŃõ»Æ
C£®¼×Ķé·Ö×ÓÖŠ¾ßÓŠ¼«ŠŌ¼ü
D£®¼×Ķé·Ö×ÓÖŠĖÄøöC”ŖH¼üŹĒĶźČ«µČ¼ŪµÄ¼ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ½Ī÷Ź”øßŅ»ĻĀŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
¢ń.ijĪĀ¶ČĻĀ,ŌŚ2 LČŻĘ÷ÖŠ3ÖÖĪļÖŹ¼ä½ųŠŠ·“Ó¦,X”¢Y”¢ZµÄĪļÖŹµÄĮæĖꏱ¼äµÄ±ä»ÆĒśĻßČēĶ¼”£·“Ó¦ŌŚt1 minŹ±µ½“ļĘ½ŗā,ČēĶ¼ĖłŹ¾:
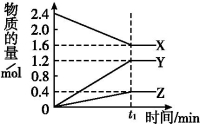
£Ø1£©øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ ”£
£Ø2£©¢ŁČōÉĻŹö·“Ó¦ÖŠX”¢Y”¢Z·Ö±šĪŖNH3”¢H2”¢N2,ĒŅŅŃÖŖ1 mol °±Ęų·Ö½ā³ÉµŖĘųŗĶĒāĘųŅŖĪüŹÕ46 kJµÄČČĮæ,ŌņÖĮt1 minŹ±,øĆ·“Ó¦ĪüŹÕµÄČČĮæĪŖ ;ŌŚ“Ėt1 minŹ±¼äÄŚ,ÓĆH2±ķŹ¾·“Ó¦µÄĘ½¾łĖŁĀŹv£ØH2£©ĪŖ ”£
¢ņ. ŃĒĮņĖįÄĘŗĶµāĖį¼ŲŌŚĖįŠŌČÜŅŗĄļ·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ£ŗ
5Na2SO3+2KIO3+H2SO4 ===5Na2SO4+K2SO4+I2+H2O£¬
øĆ·“Ó¦¹ż³ĢŗĶ»śĄķ½Ļø“ŌÓ£¬Ņ»°ćČĻĪŖ·ÖĪŖŅŌĻĀ¼ø²½£ŗ
¢ŁIO3-+SO32-”śIO2-+SO42-£ØĀż£©
¢ŚIO2-+2SO32-”śI-+2SO42-£Øæģ£©
¢Ū5I-+6H++IO3-”ś3I2+3H2O£Øæģ£©
¢ÜI2+SO32-+H2O”ś2I-+SO42-+2 H+£Øæģ£©
£Ø1£©øł¾ŻÉĻŹöĢõ¼žĶĘ²ā£¬“Ė·“Ó¦µÄ×ܵķ“Ó¦ĖŁĀŹÓÉ ²½·“Ó¦¾ö¶Ø”££ØĢī”°¢Ł”¢¢Ś”¢¢Ū”¢¢Ü”±£©”£
£Ø2£©ČōŌ¤ĻČ¼ÓČėµķ·ŪČÜŅŗ£¬ÓÉĢāŹöæ“,±ŲŠėŌŚ Ąė×ÓĻūŗÄĶźŹ±£¬²Å»įŹ¹µķ·Ū±äĄ¶µÄĻÖĻó²śÉś”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ½Ī÷Ź”ø߶žĻĀŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŹµŃéĢā
Ä³ŃŠ¾æŠŌѧĻ°Š”×éµÄĶ¬Ń§ĄūÓĆĻĀĮŠ×°ÖĆ½ųŠŠŅŅ“¼“ß»ÆŃõ»ÆµÄŹµŃ锣Ēė·ÖĪö»Ų“š£ŗ


£Ø1£©ĒėŠ“³öŹµŃé¹ż³ĢÖŠµÄ×ܵĻÆѧ·“Ó¦·½³ĢŹ½____________________________________”£
£Ø2£©ŌŚ²»¶Ļ¹ÄČėæÕĘųµÄĒéæöĻĀ£¬ŅĘČ„¾Ę¾«µĘ£¬·“Ó¦ČŌÄܼĢŠų½ųŠŠ£¬ĖµĆ÷ŅŅ“¼µÄ“ß»ÆŃõ»Æ·“Ó¦ŹĒ________·“Ó¦”£½ųŅ»²½ŃŠ¾æ±ķĆ÷£¬¹ÄĘųĖŁ¶ČÓė·“Ó¦ĢåĻµµÄĪĀ¶Č¹ŲĻµĒśĻßČēÉĻĶ¼ĖłŹ¾”£¹ÄĘųĖŁ¶Č¹żæģ£¬·“Ó¦ĢåĻµĪĀ¶Č·“¶ųĻĀ½µµÄŌŅņ___________________________”£
£Ø3£©·“Ó¦½ųŠŠŅ»¶ĪŹ±¼äŗó£¬øÉŌļŹŌ¹ÜaÖŠÄÜŹÕ¼Æµ½²»Ķ¬µÄĪļÖŹ£¬ĖüĆĒŹĒ_________________”£¼ÆĘųĘæÖŠŹÕ¼Æµ½µÄĘųĢåµÄÖ÷ŅŖ³É·ÖŹĒ_______________”£
£Ø4£©ŌŚ¼ģŃéÉś³ÉĪļµÄ¹ż³ĢÖŠ£¬Ņ»Ī»Ķ¬Ń§ŗÜÅ¼Č»µŲ·¢ĻÖĻņäåĖ®ÖŠ¼ÓČėŅŅČ©ČÜŅŗ£¬äåĖ®ĶŹÉ«”£Õė¶ŌäåĖ®ĶŹÉ«µÄŌŅņ£¬øĆŠ”×éµÄĶ¬Ń§ĆĒ¾¹ż·ÖĪöŗó£¬Ģį³öĮ½ÖÖ²ĀĻė£ŗ
¢ŁäåĖ®½«ŅŅČ©Ńõ»ÆĪŖŅŅĖį£»¢ŚäåĖ®ÓėŅŅČ©·¢Éś¼Ó³É·“Ó¦”£
ĒėÄćÉč¼ĘŅ»øö¼ņµ„µÄŹµŃ飬Ģ½¾æÄÄŅ»ÖÖ²ĀĻėÕżČ·£æ________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ½ĖÕŹ”ŃļÖŻŹŠø߶žŃ”ŠŽĻĀѧʌʌĩµ÷ŃŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
»ÆѧÓė»·¾³”¢²ÄĮĻµČ¹ŲĻµĆÜĒŠ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®¼ĘĖ滜Š¾Ę¬µÄÖ÷ŅŖ³É·ÖŹĒ¶žŃõ»Æ¹č
B£®µāŃĪÄÜ·ĄÖĪµāȱ·¦²”£¬µ«±ŲŠėæĘѧŗĻĄķÉćČė
C£®ÓƵē¶Ę·ĻĖ®Ö±½Ó¹ąøČÅ©Ģļ£¬æÉĢįøßĖ®×ŹŌ“µÄĄūÓĆĀŹ
D£®CO2ŹĒµ¼ÖĀĖįÓź·¢ÉśµÄÖ÷ŅŖŌŅņ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com