
| A、①③⑥ | B、④⑤⑥ |
| C、①②④ | D、①⑥ |
| m |
| M |
| 21g |
| 14g/mol |
| m |
| M |
| 2g |
| 20g/mol |


科目:高中化学 来源: 题型:
 1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125℃,反应装置如图,下列对该实验的描叙错误的是( )
1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125℃,反应装置如图,下列对该实验的描叙错误的是( )| A、为使受热均匀,可改用水浴加热 |
| B、长玻璃管冷凝回流作用 |
| C、提纯乙酸丁酯需要经过水、饱和碳酸钠溶液洗涤 |
| D、加入过量乙酸可以提高1-丁醇的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、所得溶液中的c (H+)=10-13 mol.L-1 |
| B、所得溶液中由水电离产生的c(OH -)=10-13mol.L-1 |
| C、所得溶液中的c (Mg2+)=5.6×l0-10 mol.L-1 |
| D、所加烧碱溶液的pH=13.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
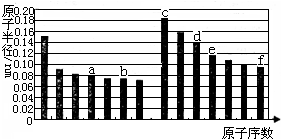
| A、a的单质在高温条件下能置换出e的单质,说明非金属性a<e |
| B、b、d两种元素的离子半径相比,前者较大 |
| C、由b、e两种元素组成的化合物能溶解于强碱溶液,但不能与酸溶液反应 |
| D、由c、d分别与f组成的化合物中的化学键类型相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、次氯酸的结构式:H-Cl-O |
B、O2的电子式: |
| C、葡萄糖的实验式:CH2O |
| D、能说明碳酸钙为强电解质的表达式:CaCO3(s)?Ca2+(aq)+CO32-(aq) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
 火柴头上通常含有氯酸钾、二氧化锰、硫等物质.某研究性学习小组进行火柴头中有关物质的实验探究.
火柴头上通常含有氯酸钾、二氧化锰、硫等物质.某研究性学习小组进行火柴头中有关物质的实验探究.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com