
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山东省济宁市金乡一中高一2月月考化学试卷(带解析) 题型:填空题
(13分)试根据下表填空:
| A | | | ||||||||||||||||
| | B | | | C | D | E | F | | ||||||||||
| G | H | I | J | | L | K | M | |||||||||||
| | | | | | | | N | | | Q | | | | | | | | |


查看答案和解析>>
科目:高中化学 来源:2011-2012学年北京市重点中学高二上学期期中考试化学(文)试卷 题型:填空题
(6分)环境和材料是现在社会中两大关注的问题,请回答:
(1)室内空气污染物主要包括CO、CO2、HCHO(甲醛)、C6H6(苯)等,在这四种污染物中,由建筑和装修产生的是_____________________。
(2)造成水体富营养化的主要原因是 。
A.汞(Hg)、镉(Cd) B.N、P的化合物
C.石油泄漏 D .工厂
.工厂 排放酸、碱、盐
排放酸、碱、盐
(3)造成白色污染的主要原因是 。
A.废塑料制品 B.废铝制易拉罐
B.废旧电池 D.生活垃圾
(4)为了治理汽车尾气的污染问题,可以在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成CO2和N2,写出该反应的化学方程式: 。
(5)合金是被广泛应用的金属材料,下列有关合金性质的说法正确的是 (填字母)
A.合金的熔点一般比它的成分金属高
B.合金的硬度一般比它的成分金属低
C.组成合金的元素种类 相同,合金的性能就一定相同
相同,合金的性能就一定相同
D.合金与各成分金属相比,具有许多优良的 物理、化学或机械性能
物理、化学或机械性能
(6)塑料、合成橡胶和 是常说的三大合成材料。
查看答案和解析>>
科目:高中化学 来源:2015届山东省济宁市高一2月月考化学试卷(解析版) 题型:填空题
(13分)试根据下表填空:
A
B C D E F
G H I J L K M
N Q
(1)请写出元素Q的基态原子电子排布式 ;元素N在周期表中的位置 周期 族。
(2)基态D原子核外有 个未成对电子;D2分子中分别有 个, 个π键。
(3)化合物DA5中既含离子键,又含共价键和配位键,请写出它的电子式 。
(4)表四中的元素能形成XY2型的共价分子有CE2、CL2、BK2、LE2四种,其分子的空间构型中有一种与其他三种不同,它是 (填化学式);而形成XY3型的共价分子也有四种,它们分别是DA3、DF3、DK3、LE3,其分子的空间构型中也有一种与其他三种不同,它是 (填化学式),它是由_ 键(填“极性”或“非极性”,下同)构成的 分子。
(5)第三周期8种元素按单质熔点高低的顺序如右图所示,其中序号“8”所代表的元素是 (填元素符号);其中气态氢化物稳定性最强的元素是 (填下图中的序号)。

(6)科学家证实,IK3属于共价化合物,分子式为I2K6,其结构式为下列四种中的一种,你认为正确的结构式是____________。
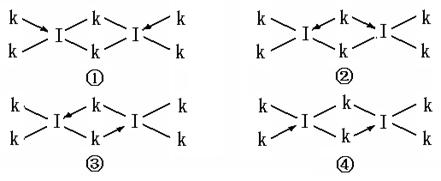
(7)向Q的硫酸盐溶液中加入足量的DA3的水溶液过程中,请写出发生反应的离子方程式 ;最后生成配离子的结构式为 。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年福建省高三下学期第六次模拟考试(理综)化学部分 题型:填空题
【化学—物质结构与性质】
氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要作用。
请回答下列问题。
(1)砷原子外围电子排布式为 。
(2)熔沸点:NH3 PH3(>、<、=)原因是
(3)N、P、As三种元素电负性由小到大的顺序为 ,NCl3分子中中心原子的杂化方式为 。
(4)汽车尾气中CO和NO经催化剂作用变成N2和CO2,此反应中三种元素第一电离能由小到大的顺序为 ,在这四种物质中含有极性键的非极分子内 键和
键和 键的比为
。
键的比为
。
(5)K3[Fe(CN)6]配合物中微粒的相互作用力有 ,配位体为 。
A.氢键 B.离子键 C.共价键 D.配位键[ E.范德华力
(6)CO、NH3都能提供孤电子对与Cu+形成配合物。Cu+与NH3形成的配合物可表示为
[Cu(NH3)n]+。该配合物中,Cu+的4s轨道及4p轨道通过sp杂化接受NH3提供的孤电子对,则[Cu(NH3)n]+中n的值为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com