
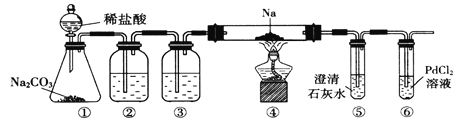
【题目】实验室验证钠能与二氧化碳发生反应,并确定其产物的装置如图所示,(已知:PdC12溶液遇CO能产生黑色的Pd),下列说法错误的是( )
A. 装置①的仪器还可以制取H2气体
B. 装置⑤中石灰水变浑浊后,再点燃酒精灯
C. 装置②③中分别盛装饱和Na2CO3溶液、浓H2SO4
D. 装置⑥中有黑色沉淀,发生的反应是PdC12+CO+H2O=Pd↓+CO2+2HC1
【答案】C
【解析】
由实验装置图可知,装置①为二氧化碳制备装置,装置②中盛有饱和碳酸氢钠溶液,用以除去二氧化碳中的氯化氢,装置③中盛有浓硫酸,用以除去水蒸气,装置④为钠与干燥二氧化碳在加热条件下发生反应的装置,装置⑤为二氧化碳的检验装置,装置⑥为一氧化碳的检验和吸收装置。
A项、装置①为固体和液体不加热反应制备气体的装置,锌和稀硫酸反应制氢气可以用装置①,故A正确;
B项、金属钠易与空气中的氧气、水蒸气等发生反应,实验之前,应用二氧化碳气体排出装置中的空气,当装置⑤中石灰水变浑浊后,说明空气已排净,再点燃酒精灯,可排除氧气、水蒸气等对钠与二氧化碳反应的干扰,故B正确;
C项、装置①中反应产生的二氧化碳气体含有氯化氢和水蒸气,因为碳酸钠溶液与二氧化碳反应,应先用饱和碳酸氢钠溶液除去二氧化碳气体中的氯化氢,故C错误;
D项、根据题给信息可知,PdC12溶液与CO发生氧化还原反应生成黑色的Pd、二氧化碳和氯化氢,反应的化学方程式为PdC12+CO+H2O=Pd↓+CO2+2HC1,故D正确。
故选C。


 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列叙述不正确的是
A.28gN2所含分子数为NA
B.0.2 mol/L Na2SO4中所含Na+ 数为0.4NA
C.标准状况下11.2L H2中所含原子数为NA
D.0.5mol CH4和1mol H2O中所含氢原子数均为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第三周期元素,浓度均为0.01mol/L的最高价氧化物对应水化物的pH与原子半径的关系如图所示。则下列说法正确的是( )

A.气态氢化物的稳定性:N>R
B.Z的最高价氧化物对应的水化物能溶于稀氨水
C.Y和R形成的化合物既含离子键又含共价键
D.X和M两者最高价氧化物对应的水化物反应后溶液的pH>7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaCl是我们生活中必不可少的物质。将NaCl固体溶于水,溶解过程如图所示,下列说法正确的是
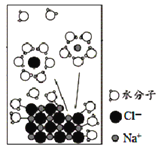
A.该过程发生了分解反应
B.离子从固体表面脱离后不会再回到固体表面
C.水合Na+的图示不科学
D.NaCl溶于水后发生了电离,是在通电条件下进行的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于离子的检验说法正确的是
A.向某溶液中滴入足量盐酸,如观察到无色无味的气体产生,且能使澄清石灰水变浑浊,即证明溶液中必定有![]()
B.向某无色溶液中加入BaCl2溶液,有白色沉淀出现,再加入稀盐酸,沉淀不消失,无法证明溶液一定含有![]()
C.向某无色溶液中加入少量稀氢氧化钠溶液后,用湿润的红色石蕊试纸靠近试管口,若试纸不变蓝,则说明该溶液中无![]()
D.如透过蓝色的钴玻璃能够观察到紫色火焰,则一定有钾元素,一定不含有钠元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】拉曼光谱证实,AlO2-在水中转化为[Al(OH)4]-。将一定量的Na2CO3、NaAlO2固体混合物溶于适量水中,再逐滴加入1mol/L盐酸,测得溶液中CO32-、HCO3-、[Al(OH)4]-、Al3+的物质的量与加入盐酸的体积变化关系如图所示,则下列说法正确的是

A.CO32-、HCO3-和[Al(OH)4]-在水溶液中可大量共存
B.d线表示的反应为:[Al(OH)4]-+H+=Al(OH)3↓+H2O
C.原固体混合物中CO32-与AlO2-的物质的量之比为1:1
D.V1=150mL,V2=300mL;M点生成的CO2为0.05mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用氯氧化法处理含氰(CN-)废水,一定条件下,氯气和CN-反应生成无毒气体N2和CO2。下列说法不正确的是( )
A.CN-中碳元素的化合价为+2B.该反应的氧化产物是N2
C.反应中氧化剂和还原剂的系数比为5:2D.该反应的还原产物为Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图装置中发生反应的离子方程式为:Zn+2H+=Zn2++H2↑,下列说法错误的是

A. a、b不可能是同种材料的电极
B. 该装置可能是电解池,电解质溶液为稀盐酸
C. 该装置可能是原电池,电解质溶液为稀盐酸
D. 该装置可看作是铜-锌原电池,电解质溶液是稀硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数依次递增且都小于36的X、Y、Z、Q、W五种元素,其中X是原子半径最小的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Q原子基态时2p原子轨道上有2个未成对的电子,W元素的原子结构中3d能级有4个未成对电子。回答下列问题:
(1)Y2X2分子中Y原子轨道的杂化类型为____, Y2X2分子中σ键和π键个数比为_______ 。
(2)化合物ZX3的沸点比化合物YX4的高,其主要原因是_____。
(3)元素Y的一种氧化物与元素Z的一种氧化物互为等电子体,元素Z的这种氧化物的分子式是_______。
(4)元素W能形成多种配合物,如:W(CO)5等。
①基态W3+的M层电子排布式为______。
②W(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断W(CO)x晶体属于________(填晶体类型)。
(5)下列有关的说法正确的是________________。
A.分子晶体中,共价键键能越大,该分子晶体的熔沸点越高
B.电负性顺序:X<Y<Z<Q
C.因为晶格能CaO比KCl高,所以KCl比CaO熔点低
D.H2YO3的分子结构中含有一个非羟基氧,故其为中强酸
(6)Q和Na形成的一种只含有离子键的离子化合物的晶胞结构如图,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为_____。已知该晶胞密度为ρ g/cm3,阿伏加德罗常数为NA,求晶胞边长a=_____cm。(用含ρ、NA的计算式表示)

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com