
| A£® | CO2ŹĒŃõ»Æ²śĪļ | |
| B£® | H2C2O4ŌŚ·“Ó¦ÖŠ±»Ńõ»Æ | |
| C£® | 1mol KClO3²Ī¼Ó·“Ó¦£¬×ŖŅʵĵē×ÓĪŖ1mol | |
| D£® | H2C2O4µÄŃõ»ÆŠŌĒæÓŚClO2µÄŃõ»ÆŠŌ |
·ÖĪö 2KClO3+H2C2O4+H2SO4=2ClO2”ü+K2SO4+2CO2”ü+2H2O£ØO¾łĪŖ-2¼Ū£©ÖŠ£¬ClŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ+5¼Ū½µµĶĪŖ+4¼Ū£¬CŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ+3¼ŪÉżøßµ½+4¼Ū£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗA£®øĆ·“Ó¦ÖŠCŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ+3¼ŪÉżøßµ½+4¼Ū£¬ĖłŅŌ²ŻĖįŹĒ»¹Ō¼Į£¬Ōņ¶žŃõ»ÆĢ¼ŹĒŃõ»Æ²śĪļ£¬¹ŹAÕżČ·£»
B£®øĆ·“Ó¦ÖŠ²ŻĖįŹĒ»¹Ō¼Į£¬ŌŚ·“Ó¦ÖŠ±»Ńõ»Æ£¬¹ŹBÕżČ·£»
C.1molKClO3²Ī¼Ó·“Ó¦ÓŠ1mol”Į£Ø5-4£©=1molµē×Ó×ŖŅĘ£¬¹ŹCÕżČ·£»
D£®øĆ·“Ó¦ÖŠ²ŻĖįŹĒ»¹Ō¼Į£¬¶žŃõ»ÆĀČŹĒ»¹Ō²śĪļ£¬ĖłŅŌ²ŻĖįµÄ»¹ŌŠŌ“óÓŚClO2µÄ»¹ŌŠŌ£¬¹ŹD“ķĪó£®
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éŃõ»Æ»¹Ō·“Ó¦£¬ĪŖøßæ¼³£¼ūĢāŠĶ£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦µÄ漲飬ӊĄūÓŚÅąŃųѧɜµÄ»ÆѧæĘѧĖŲŃų£¬ÄŃ¶Č²»“ó£¬×¢Ņā“ÓŌŖĖŲ»ÆŗĻ¼ŪµÄ½Ē¶ČŹ¶±šĻą¹ŲøÅÄī”¢ÅŠ¶ĻĪļÖŹµÄŠŌÖŹ£®


 ĆæČÕ10·ÖÖÓæŚĖćŠÄĖćĖŁĖćĢģĢģĮ·ĻµĮŠ“š°ø
ĆæČÕ10·ÖÖÓæŚĖćŠÄĖćĖŁĖćĢģĢģĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 °“ŅŖĒóĶź³ÉĻĀĮŠĪŹĢā£ŗ
°“ŅŖĒóĶź³ÉĻĀĮŠĪŹĢā£ŗ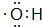 £»
£»²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.75mol | B£® | 1.25mol | C£® | 1.5mol | D£® | 2mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·ūŗĻĶØŹ½CnH2nO3 | B£® | ŗĶŅŅ“¼ÖŠ»Æѧ¼üĄąŠĶĻąĶ¬ | ||
| C£® | ÄÜŗĶ½šŹōÄĘ·“Ó¦ | D£® | ÄÜŹ¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ł·āČż³ß | B£® | ĶæÖ¬ÄØ·Ū | C£® | ɳĄļĢŌ½š | D£® | »šÉĻ½½ÓĶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com