
| A. | 氯化钠的电子式: | |
| B. | 过氧化钠的化学式:Na2O | |
| C. | Cl-的结构示意图: | |
| D. | 硫酸的电离方程式:H2SO4=2H++SO42- |
分析 A.氯化钠为离子化合物,阴离子氯离子必须标出所带电荷;
B.过氧化钠的化学式中含有2个O;
C.氯离子的核电荷数为17,核外电子总数为18,最外层为8个电子;
D.硫酸为强电解质,在溶液中完全电离出氢离子和硫酸根离子.
解答 解:A.氯化钠为离子化合物,其中氯离子必须标出所带电荷,氯化钠的电子式为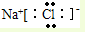 ,故A错误;
,故A错误;
B.Na2O为氧化钠的化学式,过氧化钠的化学式为Na2O2,故B错误;
C.氯离子的最外层达到8电子稳定结构,正确的离子结构示意图为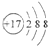 ,故C错误;
,故C错误;
D.硫酸在溶液中完全电离,其电离方程式为H2SO4=2H++SO42-,故D正确;
故选D.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及离子结构示意图、电子式、离子结构示意图、化学式等知识,明确常见化学用语的表示方法为解答关键,试题培养了学生的规范答题能力.


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:填空题
 某研究小性学习小组的同学欲用如图所示的装置完成下列实验,验证制得的乙烯气体中含有SO2、CO2、水蒸气;确定乙烯与单质溴能否反应及反应类型.
某研究小性学习小组的同学欲用如图所示的装置完成下列实验,验证制得的乙烯气体中含有SO2、CO2、水蒸气;确定乙烯与单质溴能否反应及反应类型.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可以用聚氯乙烯制的薄膜来包装药品和食品 | |
| B. | 酒精杀菌消毒利用的是使蛋白质盐析的原理 | |
| C. | 碘是人体必需的微量元素之一,有“智力元素”之称 | |
| D. | 医疗垃圾中含有多种致病微生物,因此一般采用卫生填埋的方法来处理 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 保存液溴时用水封 | |
| B. | 用待测液润洗滴定用的锥形瓶 | |
| C. | 用稀盐酸洗涤做过银镜反应的试管 | |
| D. | 配制FeCl3溶液时,向溶液中加入少量Fe和稀盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | H2(g)+CO(g)?C(s)+H2O(g)△H>0 | B. | 2SO3(g)?2SO2(g)+O2(g)△H>0 | ||
| C. | 4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H<0 | D. | N2(g)+3H2(g)?2NH3(g)△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 溶液的pH值变小 | |
| B. | 醋酸的电离度增大 | |
| C. | 溶液的导电能力减弱 | |
| D. | 中和此溶液所需的0.1摩/升NaOH溶液的体积增加 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠与氯气反应生成氯化钠后,其结构的稳定性增强,体系的能量升高 | |
| B. | 物质燃烧可看成“储存”在物质内部的能量(化学能)转化为热能释放出来 | |
| C. | 现在人们使用的能源正向多元化发展,许多新能源不断被开发利用,其中氢能和太阳能均属于清洁能源 | |
| D. | 需加热才能发生的反应不一定是吸收能量的反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com