
下列有关化学用语表示错误的是
A.HCN的结构式:H-C≡N B.HClO的电子式为:
C.CH4分子的球棍模型: D.2-氯甲苯的结构简式:
D.2-氯甲苯的结构简式:
 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:
某兴奋剂的结构简式如右图所示,下列有关该物质的说法正确的是 ( )
A.该物质能发生加成、取代、氧化、酯化、水解等反应
B.该物质分子中的所有氢原子可能共平面
C.滴人KMnO4(H+)溶液,可观察到紫色褪去,能证明结构中存在碳碳双键
D.1 mol该物质分别与浓溴水和H2反应时最多消耗Br2和H2分别为4 mol、7 mol

查看答案和解析>>
科目:高中化学 来源: 题型:
对下列实验现象的原因分析不正确的一项是
| 选项 | 实验现象 | 原因分析 |
| A | 浓硫酸遇湿润的蓝色石蕊试纸,先变红,后变黑 | 硫酸有酸性,使石蕊变红,浓硫酸有脱水性,使试纸炭化变黑 |
| B | 新制氯水中滴加石蕊试液,溶液先变红,后褪色 | 氯气与水反应生成HCl、HClO,HCl显强酸性,使石蕊变红,HClO具有强氧化性,使其褪色 |
| C | SO2通入溴水中,溴水褪色 | SO2具有漂白性,使其褪色 |
| D | 向湿润蔗糖中加入浓硫酸,固体迅速变黑,后体积急剧膨胀 | 在浓硫酸脱水作用下,蔗糖被炭化,炭与浓硫酸反应生成了CO2、SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.短周期元素都是主族元素
B.第ⅦA族元素从上到下,其氢化物的稳定性逐渐增强
C.同周期元素(0族除外)从左到右,原子半径逐渐减小
D.35Cl和37Cl原子核中的质子数之比为9:l0
查看答案和解析>>
科目:高中化学 来源: 题型:
2014年初,雾覆天气多次肆虐我国中东部地区。加强汽车尾气排放监测和燃煤企业的治理对于减少雾霾具有重要的意义。
(1)利用原电池工作原理测定汽车尾气中CO的浓度,其装置如图所示。该电池中电解质为熔融碳酸盐,CO32-在固体介质中可以自由移动,气体A为 ,正极发生的电极反应式 。
 (2)某化学兴趣小组用下图所示流程,测定标准状况下体积为V L的燃煤烟气中SO2的含量:
(2)某化学兴趣小组用下图所示流程,测定标准状况下体积为V L的燃煤烟气中SO2的含量:

尾气中SO2的体积分数为 (用含有V、m的代数式表示)。
(3)已知常温下弱电解质的电离平衡常数如下
| NH3·H2O | Kb=1.8×10-5mol·L-1 |
| H2SO3 | Ka1=1.2×10-2mol·L-1 Ka2=1.3×10-8mol·L-1 |
 ①若用氨水吸收工业废气中的SO2,当吸收液失去吸收能力时,则此时溶液呈 性(填“酸”“碱”或“中”)。
①若用氨水吸收工业废气中的SO2,当吸收液失去吸收能力时,则此时溶液呈 性(填“酸”“碱”或“中”)。
②在通入废气的过程中,水的电离程度如何变化 。当恰好形成正盐时,溶液中离子浓度的大小关系为 。
③可通过电解法使吸收液再生而循环利用(电极均为石墨电极),并生成化工原料硫酸。其工作示意图见右图。试写出生成硫酸的电极反应式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的转化在给定条件下能实现的是
|
|
|
|




|
|

|
|
 ②S SO3 H2SO4
②S SO3 H2SO4
|
|

 ③Cu2(OH)2CO3 CuCl2(aq) Cu
③Cu2(OH)2CO3 CuCl2(aq) Cu
|
|

 ④Fe2O3 FeCl3 无水FeCl3
④Fe2O3 FeCl3 无水FeCl3 
 ⑤饱和NaCl(aq) NaHCO3 Na2CO3
⑤饱和NaCl(aq) NaHCO3 Na2CO3
A.①③⑤ B.②③④ C.②④⑤ D.①④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列实验操作和现象所得出的结论错误的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向FeCl2溶液中通入适量Cl2 | 溶液由浅绿 色变为黄色 | 氧化性:Cl2>Fe3+ |
| B | 向某溶液中先滴加盐酸无现象,再滴加BaCl2溶液 | 有白色沉淀 生成 | 原溶液中含有SO42- |
| C | 蔗糖溶液在硫酸存在下水浴一段时间后,再与银氨溶液混合加热 | 无银镜出现 | 蔗糖没有水解 |
| D | 向无水乙醇中加入浓H2SO4,加热至170°C将产生的气体通入酸性KMnO4溶液 | 紫红色褪去 | 使溶液褪色的不一定是 乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
电子产品产生的大量电子垃圾对环境构成了极大的威胁。某化学兴趣小组将一批废弃的线路板简单处理后,得到含Cu、Al、Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
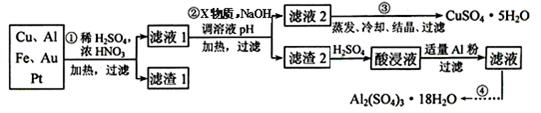
按要求回答下列问题:
(1)滤渣1中存在的金属有____________。
(2)已知沉淀物的pH如下表:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe2+ | 7.0 | 9.0 |
| Fe3+ | 1.9 | 3.7 |
| Cu2+ | 4.9 | 6.7 |
| Al3+ | 3.0 | 4.4 |
①则操作②中X物质最好选用的是___________(填编号)
a.酸性高锰酸钾溶液 b.漂白粉 c.氯气 d.双氧水
②理论上应控制溶液pH的范围是________________________。
(3)检验滤液2中既不存在Fe2+又不存在Fe3+的操作步骤是____________________。
(4)用一个离子方程式表示在酸浸液中加入适量铝粉的反应:___________________。
(5)由CuSO4·5H2O制备CuSO4时,应把CuSO4·5H2O放在 (填仪器名称)
中加热脱水。
(6)现在某些电器中使用的高铁电池是一种新型可充电电池,与普通高能电池相比,该
电池能长时间保持稳定的放电电压。高铁电池的总反应为:
3Zn + 2K2FeO4 + 8H2O 3Zn(OH)2 + 2Fe(OH)3 + 4KOH,该电池放电时负极反应式为 ,每有1mol K2FeO4被还原,转移电子的物质的量为 ,充电时阳极反应式为 。
3Zn(OH)2 + 2Fe(OH)3 + 4KOH,该电池放电时负极反应式为 ,每有1mol K2FeO4被还原,转移电子的物质的量为 ,充电时阳极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子,在强碱性溶液中可以大量共存的是:
A.Na+、Ba2+、Cl-、SO42- B. Na+、Ba2+、AlO2-、NO3-
C.NH4+、K+、Cl-、NO3- D. Na+、K+、NO3-、SiO32-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com