
【题目】根据如图所示实验装置,回答下列问题: 
(1)写出下列仪器的名称:① , ② , ④ , ⑤ .
(2)若利用装置I分离酒精和水的混合物,还缺少的仪器是;在实验中,仪器①中加入沸石的作用是;②的进水口是(填“f”或“g”).
(3)使用装置II进行的实验操作名称为 , 实验前需进行的操作为 .
(4)若在实验室中进行石油的分离实验制取汽油,应选择的实验装置是(填“I”或“II”).
【答案】
(1)蒸馏烧瓶;冷凝管;锥形瓶;分液漏斗
(2)温度计;防暴沸;g
(3)分液;检验装置气密性
(4)I
【解析】解:(1)根据仪器图象知,)①②④⑤分别是蒸馏烧瓶、冷凝管、锥形瓶、分液漏斗,所以答案是:①蒸馏烧瓶(圆底烧瓶);②冷凝器;④锥形瓶;⑤分液漏斗;(2)蒸馏时需要控制温度,所以还需要测量温度的温度计;沸石有防暴沸的作用,防止液体剧烈沸腾而产生安全事故;冷凝管中的水流采用逆流方式,所以g是进水口、h是出水口,
所以答案是:温度计;防暴沸;g;(3)该操作是分液,适用于分离互不相溶的液体,含有活塞的仪器在使用前必须检查装置的气密性,分液漏斗中含有活塞,为防止实验失败,在使用前必须检验气密性,
所以答案是:分液;检验装置的气密性(4)石油中各成分互溶且是液体,应该采用蒸馏的方法,故选I.


科目:高中化学 来源: 题型:
【题目】Na2O2具有强氧化性,H2具有还原性,某同学根据氧化还原反应的知识推测Na2O2与H2能发生反应。为了验证此推测结果,该同学设计并进行如下实验。
I.实验探究
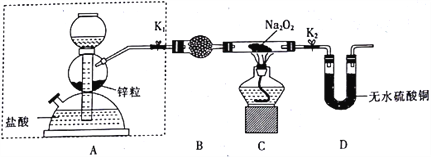
步骤1:按如图所示的装置组装仪器(图中夹持仪器已省略)并检查装置的气密性,然后装入药品。
步骤2:打开K1、K2,在产生的氢气流经装有Na2O2的硬质玻璃管的过程中,未观察到明显现象。
步骤3:进行必要的实验操作,淡黄色的粉末慢慢变成白色固体,无水硫酸铜未变蓝色。
(1)组装好仪器后,要检查装置的气密性。简述检查虚线框内装置气密性的方法:________。
(2)B装置中所盛放的试剂是_____,其作用是_______。
(3)步骤3中的必要操作为打开K1、K2,_______(请按正确的顺序填入下列步骤的字母)。
A.加热至Na2O2逐渐熔化,反应一段时间
B.用小试管收集气体并检验其纯度
C.关闭K1
D.停止加热,充分冷却
(4)由上述实验可推出Na2O2与H2反应的化学方程式为__________。
II.数据处理
(5)实验结束后,该同学欲测定C装置硬质玻璃管内白色固体中未反应完的Na2O2含量。
其操作流程如下:
![]()
①测定过程中需要的仪器除固定、夹持仪器外,还有电子天平、烧杯、酒精灯、蒸发皿和____。
②在转移溶液时,若溶液转移不完全,则测得的Na2O2质量分数_____(填“偏大”“偏小”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.5 L AlCl3溶液中含Cl-个数为9.03×1022个,则AlCl3溶液的物质的量浓度为( )
A. 0.1 mol·L-1 B. 1 mol·L-1 C. 3 mol·L-1 D. 1.5 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】鉴别① 硫酸镁② 氢氧化钠③ 硫酸铜④ 氯化钾四种溶液,可用先被鉴别出来的物质来鉴别剩余溶液,则被鉴别出来的物质顺序正确的是
A. ③①②④ B. ③②①④ C. ④③②① D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式书写正确的是
A. 2SO2+O2=2SO3;△H= -196.6 kJ/mol
B. 2H2(g)+O2(g)=2H2O(l);△H =-571.6 kJ
C. H2(g)+ 1/2 O2(g)=H2O(l);△H =-285.8 kJ/mol
D. C(s)+O2(g)=CO2(g);△H =+393.5kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列能使醋酸溶液中CH3COOH的电离程度增大,而电离常数不变的操作是
A. 加水稀释
B. 升高温度
C. 加少量冰醋酸
D. 加少量的CH3COONa固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列各小题
(1)氯化铁水溶液常温时pH ______7(填>或=或<),原因是(用离子方程式表示)________。把氯化铁溶液蒸干,灼烧,最后得到的固体产物是_________。
(2)用离子方程式表示泡沫灭火器灭火原理:__________________________________________。
(3)纯碱可代替洗涤剂洗涤餐具,原因是(用离子方程式表):__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铜和浓硫酸可以在加热条件下发生如下反应(反应方程式已配平):
Cu+2H2SO4(浓) ![]() CuSO4+A↑+2H2O
CuSO4+A↑+2H2O
(1)A的化学式 , 上述反应中浓硫酸体现了(性质).
(2)一定量的铜片与100mL 18mol/L 的浓H2SO4充分反应,如果该反应过程中转移了0.2mol电子,被还原的硫酸为mol,生成的A气体在标准状况下体积为L (假设气体全部逸出).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是:
A. 将铜丝插入稀硝酸中:Cu+4H++2NO![]() ===Cu2++2NO2↑+H2O
===Cu2++2NO2↑+H2O
B. 向Fe2(SO4)3溶液中加入过量铁粉:Fe3++Fe===2Fe2+
C. 向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3·H2O===Al(OH)3↓+3NH![]()
D. 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+===H2SiO3↓+2Na+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com