
| 时间/min | CO | Zn | CO2 |
| 0 | 0.11 | 0 | 0 |
| 2 | 0.10 | 0.01 | 0.01 |
| 3 | 0.01 | 0.10 | 0.10 |
| 4 | 0.01 | 0.10 | 0.10 |
分析 (1)计算出ZnS中硫的质量分数ω(S),闪锌矿中S的质量分数为ZnS中硫的质量分数ω(S)×ω(ZnS);
根据S元素守恒:S~H2SO4,再根据质量定比关系计算;
(2)假定有2molZnS,最少通入3molO2,计算出生成的SO2的物质的量,及未反应的N2的物质的量,进而计算炉气中SO2的体积分数;
(3)CO的总转化率=$\frac{CO浓度变化量}{CO起始浓度}$×100%;
令需焦炭质量为mg,实际利用的为95%mg,由方程式可得关系式ZnO(s)~C(s),即n(ZnO)=n(C),据此计算;
(4)令生产1molZn鼓风炉中消耗空气物质的量为5y,则通入的氧气为y、制得一氧化碳为2y,实际用于还原ZnO的CO物质的量为2y×62.5%,由方程式可知,2y×62.5%=1mol;
令1molZn焙烧炉中消耗空气的物质的量为5x,根据Zn元素守恒,需ZnS1mol,根据差量法计算出从焙烧炉出来的气体物质的量变化量,利用混合气体中N2占82.5%,列方程;
两处之和即为鼓入新鲜空气.
解答 解:(1)ZnS中锌的质量分数ω(S)=$\frac{32}{97}$,则:
ω(ZnS)×$\frac{32}{97}$=16%,
故ω(ZnS)=48.5%
设生成98%硫酸为x t,则:
S~~~~~~~H2SO4
32 98
100t×16% xt×98%
所以32:98=100t×16% xt×98%
解得x=50
故答案为:48.5%;50;
(2)假定有2molZnS,最少通入3molO2,根据方程式2ZnS(s)+3O2→2ZnO(s)+2SO2 (g) 可知,生成的SO2的物质的量为2mol,未参加反应的N2的物质的量为3mol×4=12mol,此时SO2的体积分数为$\frac{2mol}{2mol+12mol}$×100%=14.3%.实际通入的空气要多,故SO2的体积分数不超过14.3%,
故答案为:14.3;
(3)由表可知,3min时反应达平衡,平衡时时CO的平衡浓度为0.01mol/L,所以CO的总转化率为$\frac{0.11mol/L-0.01mol/L}{0.11mol/L}$×100%=90.9%,
令需焦炭质量为mg,实际利用的为95%mg,由方程式可得,关系式ZnO(s)~C(s),所以n(ZnO)=n(C),即$\frac{95%mg}{12g/mol}$=1,解得m=12.6;
故答案为:90.9%;12.6;
(4)设焙烧炉中消耗空气的物质的量为5x,鼓风炉中消耗空气物质的量为5y
则:2C+O2=2CO; ZnO(s)+CO(g)=Zn(g)+CO2(g).
y 2y 2y×62.5% 1mol
所以2y×62.5%=1mol
解得 y=0.8mol,所以 5y=4mol
2ZnS+3O2=2ZnO+2SO2 △n
2mol 1mol
1mol 0.5mol
所以4x÷(5x-0.5mol)=82.5%
解得 x=3.3mol,所以 5x=16.5mol
所以5x+5y=4mol+16.5mol=20.5mol
V(空气)=20.5mol×22.4L•mol-1=459.2L
答:应向焙烧炉和鼓风炉中鼓入新鲜空气共459.2L.
点评 本题以金属冶炼为载体,考查有关化学计算,综合性大,关键要理清思路、掌握好基础知识,难度比较大.


 一线名师提优试卷系列答案
一线名师提优试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 化学反应除了生成新物质外,还伴随着能量的变化 | |
| B. | 放热反应不需加热就能发生 | |
| C. | 需要加热才能发生的反应不一定是吸热反应 | |
| D. | 化学反应是放热还是吸热,取决于反应物和生成物所具有的总能量的相对高低 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
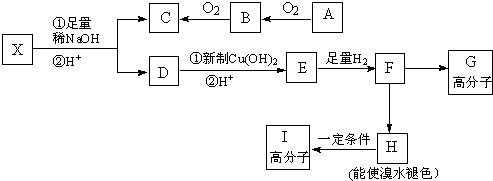
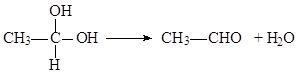
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,1 L pH=13的 Ba(OH)2溶液中含有的OH-数目为0.2NA | |
| B. | 标准状况下,2.24 L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA | |
| C. | 室温下,21.0 g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA | |
| D. | 取0.5 L 0.2 mol•L-1氯化铁溶液,所得溶液含有0.1 NA个Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素的非金属性次序为c>b>a | |
| B. | 元素a和元素b、c均能形成共价化合物 | |
| C. | 元素d和元素b、c均能形成离子化合物 | |
| D. | 元素c最高和最低化合价的代数和为4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若X是Na,则Z 的最高价一定为偶数 | |
| B. | 若X是O,则YX一定是离子化合物 | |
| C. | 若Y是O,则非金属性:Z>Y>X | |
| D. | 若Y是Na,则X Z不可能是同一主族元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
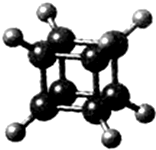
| A. | 它在核磁共振氢谱中只出现一个峰 | |
| B. | 它二氯代物有三种同分异构体 | |
| C. | 它是一种不饱和烃,既能发生取代反应,又能发生加成反应 | |
| D. | 它与苯乙烯(C6H5-CH=CH2)互为同分异构体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com