
| A. | X、Y、Z的热稳定性逐渐增强 | |
| B. | A、B、C、D只能形成5种单质 | |
| C. | A、B的氧化物的水化物的酸性逐渐增强 | |
| D. | 由B、C、D三种元素组成的化合物中只能形成共价键 |
分析 A、B、C、D四种短周期元素的原子半径依次减小,A与C核电荷数之比为3:4的两元素有Li和Be、C和O、F和Mg、Mg和S,D能分别与A、B、C形成电子总数相等的分子X、Y、Z.A为C元素,C为O元素,D为H元素,则B为N元素.X、Y、Z分别为CH4、NH3、H2O.结合元素周期律及物质性质解答.
解答 解:A、B、C、D四种短周期元素的原子半径依次减小,A与C核电荷数之比为3:4的两元素有Li和Be、C和O、F和Mg、Mg和S,D能分别与A、B、C形成电子总数相等的分子X、Y、Z.A为C元素,C为O元素,D为H元素,则B为N元素.X、Y、Z分别为CH4、NH3、H2O.
A、非金属性越强,氢化物越稳定,同周期随原子序数增大,非金属性增强,所以非金属性C<N<O,所以CH4、NH3、H2O的稳定性逐渐增强,故A正确;
B、由于C元素有非常多的同素异形体金刚石、石墨、C60、C70、C100等,氧元素只存在O2、O3等,故B错误;
C、A为碳、B为氮,最高价氧化物对应水化物分别为碳酸和硝酸,碳酸弱于硝酸,而没有指出最高价氧化物,故C错误;
D、由N、O、H三种元素组成的化合物中硝酸铵是离子化合物,故D错误;
故选:A.
点评 本题考查元素周期表及元素性质、元素周期律的有关知识,难度中等,推断元素是解题关键,A、C核电荷数关系是突破口.


 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:解答题
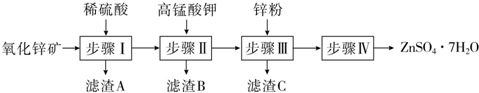
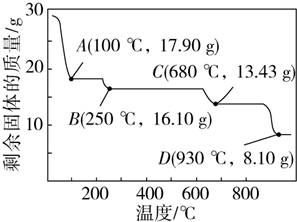
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
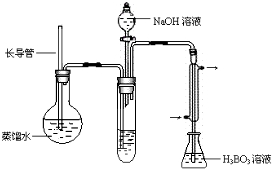
| 实验编号 | 样品和辅助试剂 | 消耗盐酸体积(mL) |
| 1 | 10.00mL溶液、0.1g催化剂、20mL浓硫酸 | 33.18 |
| 2 | 10.00mL溶液、0.1g催化剂、20mL浓硫酸 | 33.70 |
| 3 | 10.00mL溶液、0.1g催化剂、20mL浓硫酸 | 33.22 |
| 4 | x |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molCl2中含有Cl2分子的数目为NA | |
| B. | 标准状况下,22.4L水中含有水分子数目为NA | |
| C. | 含有 1molNa2SO4的溶液中含有钠离子数目为NA | |
| D. | 32gO2中含有氧原子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硫、二氧化氮、一氧化碳和二氧化碳是空气质量报告中涉及的主要污染物 | |
| B. | 正常雨水的pH等于7 | |
| C. | 二氧化硫和二氧化氮是引起酸雨的主要气体 | |
| D. | 家用汽车有利于人们出行,需要大力推广应用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
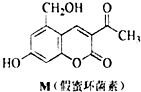
| A. | M的分子式为C12H10O5 | |
| B. | M与Br2只能发生取代反应,不能发生加成反应 | |
| C. | 1 mol M最多能与3mol NaOH反应 | |
| D. | M既能与FeCl3溶液发生反应,也能与CH3COOH发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
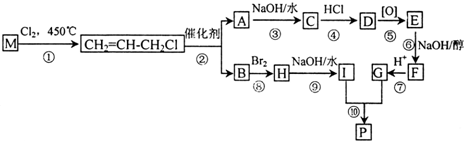
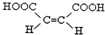 .
.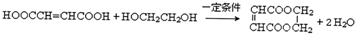 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 麦芽糖和蔗糖的水解产物相同 | |
| B. | 用新制的氢氧化铜可区分乙醇、乙醛 | |
| C. | 用高锰酸钾酸性溶液可以区分苯、甲苯 | |
| D. | 用饱和溴水可区分苯酚溶液、己烷、1-己烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
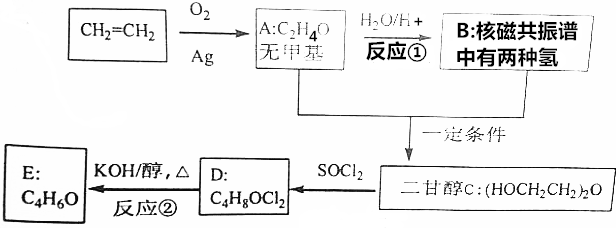
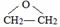 DClCH2CH2OCH2CH2Cl;
DClCH2CH2OCH2CH2Cl;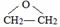 +H2O$\stackrel{H+}{→}$HOCH2CH2OH;反应②ClCH2CH2OCH2CH2Cl+2KOH$→_{△}^{醇}$CH2=CHOCH=CH2+2KCl+2H2O;
+H2O$\stackrel{H+}{→}$HOCH2CH2OH;反应②ClCH2CH2OCH2CH2Cl+2KOH$→_{△}^{醇}$CH2=CHOCH=CH2+2KCl+2H2O;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com