
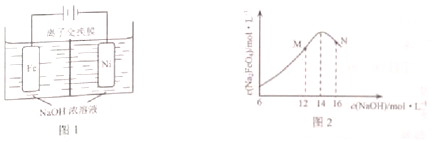
分析 (1)与汽油相比,氢气作为燃料的优点有污染小、可再生、来源广、资源丰富、燃烧热值高等;碱性氢氧燃料电池的负极反应式为H2+2OH--2e-=2H2O;
(2)①H2(g)+A(l)=B(l)△H1,②O2(g)+B(l)=A(l)+H2O2(l)△H2,两反应的△S<0,根据△G=△H-T△S,因为均为两反应自发反应,因此△H均小于0,将①+②得:H2(g)+O2(g)=H2O2(l)的△H=△H1+△H1<0;
(3)MHx(s)+yH2(g)?MHx+2y(s)△H<0,该反应属于气体的物质的量发生变化的反应,a.平衡时气体的物质的量不变,容器内气体压强保持不变;b.该反应为可逆反应,不能完全转化,吸收ymol H2需大于1mol MHx;c.若降温,平衡正向移动,该反应的平衡常数增大;d.若向容器内通入少量氢气,相当于增大压强,平衡正向移动,则v(放氢)<v(吸氢);
(4)利用太阳能直接分解水制氢,是将光能转化为化学能;
(5)氢气具有还原性,根据题意Na2FeO4只在强碱性条件下稳定,易被H2还原.电解过程中,须将阴极产生的气体及时排出,防止Na2FeO4与H2反应使产率降低.
解答 解:(1)与汽油相比,氢气作为燃料的优点有污染小、可再生、来源广、资源丰富、燃烧热值高等;碱性氢氧燃料电池的负极反应式为H2+2OH--2e-=2H2O,
故答案为:污染小、可再生、来源广、资源丰富、燃烧热值高;H2+2OH--2e-=2H2O;
(2)①H2(g)+A(l)=B(l)△H1,②O2(g)+B(l)=A(l)+H2O2(l)△H2,两反应的△S<0,根据△G=△H-T△S,因为均为两反应自发反应,因此△H均小于0,将①+②得:H2(g)+O2(g)=H2O2(l)的△H=△H1+△H2<0,
故答案为:<;
(3)MHx(s)+yH2(g)?MHx+2y(s)△H<0,该反应属于气体的物质的量发生变化的反应,a.平衡时气体的物质的量不变,容器内气体压强保持不变,正确;b.该反应为可逆反应,不能完全转化,吸收ymol H2需大于1mol MHx,错误;c.若降温,平衡正向移动,该反应的平衡常数增大,正确;d.若向容器内通入少量氢气,相当于增大压强,平衡正向移动,则v(放氢)<v(吸氢),错误;
故答案为:ac;
(4)利用太阳能直接分解水制氢,是将光能转化为化学能,
故答案为:将光能转化为化学能;
(5)氢气具有还原性,根据题意Na2FeO4只在强碱性条件下稳定,易被H2还原.电解过程中,须将阴极产生的气体及时排出,防止Na2FeO4与H2反应使产率降低,
故答案为:防止Na2FeO4与H2反应使产率降低.
点评 本题主要考查了化学反应中的能量变化、化学平衡状态的判断、电解原理及其应用的相关知识,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 等物质的量浓度的NH4Cl溶液与(NH4)2SO4溶液相比,前者的c(H+)更小 | |
| B. | 0.1 mol•L-l的CH3COONa溶液中:c(CH3COO-)+c(CH3COOH)>0.1 mol•L-1 | |
| C. | pH=9.4,浓度均为0.l mol•L-1的HCN与NaCN的混合溶液中:c(Na+)>c(HCN)>c(CN-)>c(OH-) | |
| D. | 将少量AgCl分别加入等体积等物质的量浓度的NaBr溶液与KI溶液中,充分反应后,后者的c(Ag+)更大 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
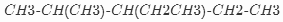 的名称是2-甲基-3-乙基戊烷.
的名称是2-甲基-3-乙基戊烷. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将2.4g炭完全转化为水煤气,然后再充分燃烧,整个过程放出热量39.35kJ | |
| B. | C的燃烧热为-110.5kJ/mol | |
| C. | H2的燃烧热为-241.8kJ/mol | |
| D. | 由反应③可知,反应过程中转移5mol电子且生成液态水时放出的热量大于604.5kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
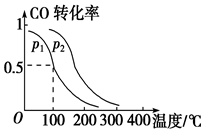 运用化学反应原理研究物质的性质具有重要意义.请回答下列问题:
运用化学反应原理研究物质的性质具有重要意义.请回答下列问题:| Ka1 | Ka2 | |
| H2SO3 | 1.3×10-2 | 6.3×10-8 |
| H2CO3 | 4.2×10-7 | 5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时正极上的电极反应为:Li-e-═Li+ | |
| B. | 该充电宝的凝胶介质可用KOH水溶液代替 | |
| C. | 充电时每生成14g Li,凝胶介质中有2mol电子通过 | |
| D. | 充电时电池的正极失电子后Li4V2O3会转化为V2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com