
| A、1 | B、2 | C、3 | D、4 |


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:
| A、2.1g | B、3.6g |
| C、7.2g | D、无法求解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入AgNO3溶液和稀HNO3,看是否有浑浊出现 |
| B、加入BaCl2溶液和稀HCl,看是否有浑浊出现 |
| C、先加过量的BaCl2溶液和稀HNO3,取上层清液再加AgNO3溶液,看是否有浑浊出现 |
| D、先加过量的Ba(NO3)2溶液和稀HNO3,取上层清液再加AgNO3溶液,看是否有浑浊出现 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 50mL 0.50mol?L-1盐酸与50mL 0.55mol?L-1 NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中的热量可计算中和热.回答下列问题:
50mL 0.50mol?L-1盐酸与50mL 0.55mol?L-1 NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中的热量可计算中和热.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学键 | P-P | P-O | OO | PO |
| 键能(kJ?mol-1) | 198 | 360 | 498 | X |

查看答案和解析>>
科目:高中化学 来源: 题型:
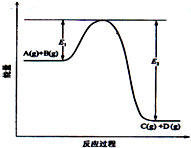 反应A(g)+B(g) 错误!未找到引用源C(g)+D(g)过程中的能量变化如图所示,请回答下列问题:
反应A(g)+B(g) 错误!未找到引用源C(g)+D(g)过程中的能量变化如图所示,请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com