

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
| NO | - 4 |
| ²āŹŌŹ±¼ä/h | 0 | 1 | 2 | 3 | 4 | 6 | 6 |
| Ńł±¾µÄPh | 4.93 | 4.72 | 4.63 | 4.58 | 4.56 | 4.55 | 4.55 |

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
 ¢ń¹¤ŅµÉĻ³£ĄūÓĆ“×ĖįŗĶŅŅ“¼ŗĻ³ÉÓŠ»śČܼĮŅŅĖįŅŅõ„£ŗCH3COOH£Øl£©+C2H5OH£Øl£©
¢ń¹¤ŅµÉĻ³£ĄūÓĆ“×ĖįŗĶŅŅ“¼ŗĻ³ÉÓŠ»śČܼĮŅŅĖįŅŅõ„£ŗCH3COOH£Øl£©+C2H5OH£Øl£©| ÅØH2SO4 |
| ”÷ |
| ĪĀ¶Č/”ę | 400 | 500 | 800 |
| Ę½ŗā³£ŹżK | 9.94 | 9 | 1 |
| n£ØCO£© | n£ØH2O£© | n£ØH2£© | n£ØCO2£© | |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 3 | 3 | 0 | 0 |
| D | 0.5 | 2 | 1 | 1 |
| E | 3 | 1 | 2 | 1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ±±¾©ŹŠ³ÆŃōĒų2009Äźøßȿğ¼¶2ŌĀĶ³Ņ»æ¼ŹŌ»ÆѧŹŌ¾ķ ĢāŠĶ£ŗ022
¾Ż±ØµĄÄ³Š©¼ņµ„µÄ²»±„ŗĶÓŠ»śĪļÓėCOŌŚµĶĪĀ”¢µĶŃ¹¼°“ß»ÆĢõ¼žĻĀæÉŅŌ×Ŗ±äĪŖĘäĖüÓŠ»śĪļ£¬Čē£ŗ
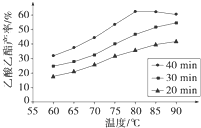
¹¤ŅµÉĻŅŌA¼°COµČĪŖŌĮĻ¾ČēĻĀµÄ·“Ó¦£¬æÉŅŌÖĘČ”¾ßÓŠÓÅĮ¼ŠŌÄܵÄŗĻ³ÉŹ÷Ö¬¼°ĶæĮĻš¤ŗĶ¼ĮµČøß·Ö×Ó²ÄĮĻ£®·“Ó¦¹ż³ĢČēĻĀĶ¼ĖłŹ¾£ŗ

ĘäÖŠAĘųĢåŌŚ¹¤ŅµÉĻÓĆÓŚŗø½Ó»ņĒŠøī½šŹō£»ŅūÓĆĮĖŗ¬ÓŠDµÄ¼Ł¾Ę£¬æÉÄÜŅżĘšŹ§Ć÷»ņĖĄĶö£»FŹĒŅ»ÖÖŗĻ³ÉŹ÷Ö¬£¬ÓĆÓŚÖʱøĖÜĮĻŗĶŗĻ³ÉĻĖĪ¬£®
»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)FµÄ½į¹¹¼ņŹ½ŹĒ__________________£®
(2)B·Ö×ÓÖŠŗ¬Ńõ¹ŁÄÜĶŵÄĆū³Ę________£®
(3)B£«D”śGµÄ·“Ó¦ĄąŠĶŹĒ___________£®
(4)Š“³ö·“Ó¦¢ņµÄ»Æѧ·½³ĢŹ½_________£®
(5)ŅŃÖŖGµÄŅ»ĄąĶ¬·ÖŅģ¹¹ĢåÄÜ·¢ÉśŅų¾µ·“Ó¦£¬ĻÖČ”0.5 moløĆĄąĶ¬·ÖŅģ¹¹ĢåÖŠÄܲśÉśŅų×ī¶ąµÄŅ»ÖÖ£¬Óė×ćĮæµÄŅų°±ČÜŅŗ³ä·Ö·“Ó¦£¬Éś³ÉŅųµÄÖŹĮæ×ī¶ąĪŖ________g£®
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com