
��2X+O2====2M ��2Y+O2====2Q ��2Z+O2====2R
��������ʽ�г���������������ʾ�Ϊ�������ͨ��״����X��Y��Z�������壬�����Ҫ��ش����⣺
��1�������Ӧ���ڳ��³�ѹ�¼���˳�����У���M�Ļ�ѧʽ��________________��
��2�������Ӧ����һ��ȼ�շ�Ӧ����Q�ĵ���ʽ��________�������Ϊ________������Է��ӡ��Ǽ��Է��ӡ�����
��3�������Ӧ�����ڴ������ڲ����������½��У���Z�Ļ�ѧʽ��____________�������ľ�������Ϊ________________��
��.��4����6.2 g Na2O�ڸ��������������м��ȣ���ַ�Ӧ����ȴ���������������Ϊ7.8 g����÷�Ӧ����Ӧ�ܣ��Ļ�ѧ����ʽΪ______________________________________��
��5��ȡ43.2 g FeO�ڿ����г�ּ��ȣ���ȴ�����������������3.2 g����÷�Ӧ����Ӧ�ݣ��Ļ�ѧ����ʽΪ_______________________________________________________________��
��.��6����Ӧ�١�����������ԭ��Ӧ��������һ���Ļ��ϼ������������ĸ������Բ�ͬ�������ҳ������Ӧ��________________������ţ���������ѡ���������_________________��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��2X+O2=
��������ʽ�г���������������ʾ�Ϊ�������ͨ��״����X��Y��Z�������壬�����Ҫ��ش����⣺
(1)�����Ӧ���ڳ��³�ѹ�¼���˳�����У���M�Ļ�ѧʽ��__________________________��
(2)�����Ӧ����һ��ȼ�շ�Ӧ����Q�ĵ���ʽ��____________________�������Ϊ_________ (����Է��ӡ��Ǽ��Է��ӡ�)��
(3)�����Ӧ�����ڴ������ڲ����������½��У���Z�Ļ�ѧʽ��___________________�������ľ�������Ϊ_________��
��.(4)��
(5)ȡ
��.(6)��Ӧ�١�����������ԭ��Ӧ��������һ���Ļ��ϼ������������ĸ������Բ�ͬ�������ҳ������Ӧ��_________ (�����)��������ѡ���������___________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ᡢ�������������ѧ�γ����������ᡣ��������������ͭ��Ӧ��������ش��������⡣
��ϡ������ͬ����Ӧ��Aͬѧ���벻���������Լ����������һ��װ����ʵ�����·�Ӧ��Cu + 2HCl === CuCl2 + H2�� ���㻭����װ�õ�ʾ��ͼ��
����100 mL 18 mol��L-'��Ũ�����м��������ͭƬ������ʹ֮��ַ�Ӧ���õ�����������ʵ���________�����������������=��)0.9mol���÷�Ӧ�Ļ�ѧ����ʽ��________________��
Bͬѧ���������Ӧ��Ļ�����м��������Σ�ʹʣ���ͭƬ�����ܽ⣬��д����Ӧ�����ӷ���ʽ��________________________________________________��
(3)W g Cu��V mL������Ũ���ᷴӦ������Һ����ɫ��W g Cu��V mL ������ϡ���ᷴӦ������Һ����ɫ��������Һ��ɫ�IJ�ͬ��Cͬѧ���������Cu2+Ũ�Ȳ�ͬ����ġ����Ƿ���ͬ�� _______����ǡ���)��������_______________________��
Dͬѧ��ΪCu2+����Һ��Ӧ������ɫ�ģ���ɫ���������ɵ�NO2��Cu2+������ɵģ��������һ��ʵ��������Dͬѧ�ļ��衣д��ʵ��IJ���������ͽ��ۣ�________________��
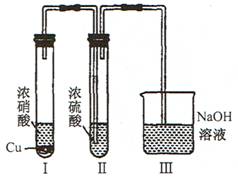
(4)EͬѧΪ̽��Ũ�����ܷ���ΪNO2����ĸ�������������ͼ��ʾ��ʵ�飬�۲쵽��������Һ��Ϊ����ɫ����δ�������ݳ�����ó��Ľ����ǣ�__________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�걱�����и������ϣ����л�ѧ�Ծ��������棩 ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com