
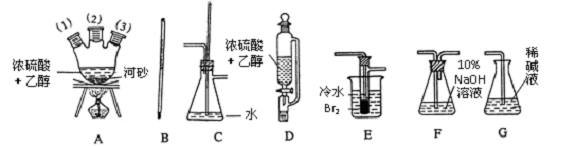
分析 (1)要制取纯净的乙烯则各装置组装顺序是:制取乙烯气体(用A、B、D组装)一安全瓶(C,兼防堵塞)→净化气体(F,用NaOH溶液吸收CO2和SO2等酸性杂质气体)→制备1,2-二溴乙烷的主要反应装置(E)→尾气处理(G)”
(2)乙醇在浓硫酸做催化剂、脱水剂,迅速加热到170度,发生消去反应生成乙烯和水;
(3)依据恒压滴液漏斗原理解答;温度计测量的是混合液的温度,应在液面以下;
(4)气流过快,锥形瓶内压强过大,会有一部分液体进入导管;
(5)溴单质易挥发,反应管E中冷水的作用是尽量减少溴的挥发;
(6)要制取纯净的乙烯,应除去含有的杂质CO2和SO2等酸性杂质气体,溴单质易挥发,容易污染空气,可用氢氧化钠吸收.
解答 解:(1)仪器组装顺序是:制取乙烯气体(用A、B、D组装:B经A(1)插入A中,D接A(2))一A(3)→安全瓶(C,兼防堵塞)→净化气体(F,用NaOH溶液吸收CO2和SO2等酸性杂质气体)→制备1,2-二溴乙烷的主要反应装置(E)→尾气处理(G)”;
故答案为:B、D、C、F、E、G;
(2)乙醇在浓硫酸做催化剂、脱水剂,迅速加热到170度,发生消去反应生成乙烯和水,反应的化学方程式:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O;
故答案为:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O;
(3)恒压滴液漏斗D内液面上方封闭气体的压强与漏斗出口下方相同,压强相同,不需要打开上面的塞子,在重力作用下液体就能流下来;反应过程中温度计测量的是混合液的温度,应在液面以下,
故答案为:不要;插入A中液面以下;
(4)气流过快,锥形瓶内压强过大,会有一部分液体进入导管,所以看到的现象为:直玻璃管中液面上升;
故答案为:直玻璃管中液面上升;
(5)溴易挥发,为减少挥发,在反应管E中加入少量水可起到水封的作用,把反应管E置于盛有冷水的小烧杯中,可降低温度,减少挥发,
故答案为:减少溴的挥发损失;
(6)要制取纯净的乙烯,应除去乙烯中含有的杂质CO2和SO2等酸性杂质气体,可以氢氧化钠溶液洗气;溴单质易挥发,容易污染空气,可用氢氧化钠吸收;
故答案为:除去乙烯中混有的CO2、SO2;吸收E中可能挥发出的溴蒸汽.
点评 本题考查了乙烯的实验室制备及性质,熟悉制备原理及注意事项是解题关键,注意熟知各种仪器的用途,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | X的能量不一定高于M的能量 | |
| B. | X和Y的总能量一定低于M和N的总能量 | |
| C. | 破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量 | |
| D. | 此反应符合质量守恒,却不符合能量守恒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3溶液与盐酸:CO32-+2 H+=H2O+CO2↑ | |
| B. | 硝酸银溶液与铜:Cu+Ag+=Cu2++Ag | |
| C. | 金属钾与水反应:K+H2O═K++OH-+H2↑ | |
| D. | 用醋酸除水垢:2CH3COOH+CaCO3=Ca2++2CH3COO-+H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | S(s)+O2(g)→SO2(g)+Q1kJ;S(g)+O2(g)→SO2(g)+Q2kJ | |
| B. | H2(g)+$\frac{1}{2}$O2(g)→H2O(l)+Q1kJ;H2(g)+$\frac{1}{2}$O2(g)→H2O(g)+Q2kJ | |
| C. | NaOH(aq)+HCl(aq)→NaCl(aq)+H2O(l)+Q1kJ NaOH(aq)+HAc(aq)→NaAc(aq)+H2O(l)+Q2kJ | |
| D. | H2(g)+Cl2(g)→2HCl(g)+Q1kJ,H2(g)+I2(g)→2HI(g)+Q2kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| W | X | |
| Y | Z |
| A. | Y的气态氢化物最稳定 | B. | Z的单核阴离子还原性最强 | ||
| C. | X单质常温下化学性质活泼 | D. | Y的原子序数比W大7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com