
【题目】下表为长式周期表的一部分其中的编号代表对应的元素.
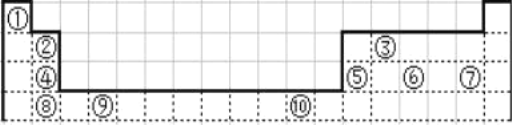
请回答下列问题:
(1)表中属于 ds 区的元素是_____(填元素符号)它的基态原子的价电子排布式为_____。
(2)表中元素①的 6 个原子与元素③的 6 个原子形成的某种平面环状分子其分子式为________,其中元素③的原子的杂化类型为_____;①和⑥形成的一种常见四原子分子的化学式为______,其立体构型为_________。
(3)某元素原子的价电子排布式为 nsnnpn+1,该元素原子的电子层上未成对电子数为_____;该元素与元素①形成的最简单分子 X 的电子式为_____。
(4)元素⑤的电负性_____④元素的电负性(选填>、=、<下同);元素⑥的第一电离能_____原子序数为 16 的元素的第一电离能。
(5)用电子式表示元素④和⑦组成的化合物的形成过程_____。
(6)上表中元素⑤的氢氧化物为两性氢氧化物,请写出元素⑤的氢氧化物与NaOH溶液反应的化学方程式:_____。
【答案】Cu 3d104s1 C6H6 sp2 PH3 三角锥形 3 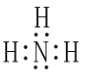 > >
> > ![]() Al(OH)3+NaOH=NaAlO2+2H2O
Al(OH)3+NaOH=NaAlO2+2H2O
【解析】
①~⑩元素分别为H、Be、C、Mg、Al、P、Cl、Ca、Ti、Cu。
(1)表中属于ds区是第IB族和IIB族元素,Cu的基态原子电子排布式为[Ar]3d104s1。
(2) 6个C原子与6个H原子形成的平面分子为苯,碳原子价层电子对数=3+0=3,H和P形成的一种常见四原子分子,先计算价层电子对数,再得立体构型。
(3)某元素原子的价电子排布式为nsnnpn+1,则n=2,该元素与元素①形成的最简单分子X为NH3。
(4)同周期,从左到右电负性逐渐增大;同周期,从左到右第一电离能具有增大趋势,但第IIA族大于第IIIA族,第VA族大于第VIA族。
(5)元素④和⑦组成的化合物为MgCl2。
(6)上表中元素⑤的氢氧化物Al(OH)3为两性氢氧化物,Al(OH)3与NaOH溶液反应生成偏铝酸钠和水。
(1)表中属于ds区是第IB族和IIB族元素,ds区元素为Cu,它的基态原子电子排布式为[Ar]3d104s1,其价电子排布式为3d104s1;故答案为:Cu;3d104s1。
(2)表中元素①的6个原子与元素③的6个原子形成的某种平面环状分子其分子式为C6H6,碳原子价层电子对数=3+0=3,因此其碳原子的杂化类型为sp2;①和⑥形成的一种常见四原子分子的化学式为PH3,价层电子对数=![]() ,因此其立体构型为三角锥形;故答案为:C6H6;sp2;PH3;三角锥形。
,因此其立体构型为三角锥形;故答案为:C6H6;sp2;PH3;三角锥形。
(3)某元素原子的价电子排布式为nsnnpn+1,则n=2,则为N,价电子排布式为2s22p3,该元素原子的电子层上未成对电子数为3;该元素与元素①形成的最简单分子X为NH3,NH3的电子式为![]() ;故答案为:3;
;故答案为:3;![]() 。
。
(4)同周期,从左到右电负性逐渐增大,因此元素⑤的电负性>④元素的电负性;同周期,从左到右第一电离能具有增大趋势,但第IIA族大于第IIIA族,第VA族大于第VIA族,元素⑥的第一电离能>原子序数为 16 的元素的第一电离能;故答案为:>;>。
(5)元素④和⑦组成的化合物为MgCl2,用电子式表示元素④和⑦组成的化合物的形成过程![]() ;故答案为:
;故答案为:![]() 。
。
(6)上表中元素⑤的氢氧化物Al(OH)3为两性氢氧化物,Al(OH)3与NaOH溶液反应的化学方程式:Al(OH)3+NaOH=NaAlO2+2H2O;故答案为:Al(OH)3+NaOH=NaAlO2+2H2O。


科目:高中化学 来源: 题型:
【题目】将有机物完全燃烧,生成CO2和H2O,将12 g该有机物完全燃烧产物通过浓硫酸,浓硫酸增重14.4 g,再通过碱石灰,又增重26.4 g。则该有机物的分子式为( )
A. C4H10 B. C2H6O
C. C3H8O D. C2H4O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H是一种香料,可用如图的设计方案合成。
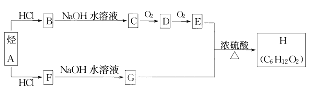
已知:①在一定条件下,有机物有下列转化关系:
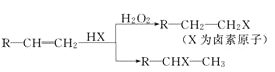
②烃A和等物质的量的HC1在不同的条件下发生加成反应,既可以生成只含有一个甲基的B,也可以生成含有两个甲基的F。
回答下列问题:
(1)D的结构简式为_______________________________________。
(2)烃A→B的化学反应方程式是____________________________________ 。
(3)F→G的化学反应类型为 _________________________________。
(4)E+G→H的化学反应方程式是 ____________________________________。
(5)H有多种同分异构体,其中含有一个羧基,且其烃基上一氯代物有两种的是 _____________(用结构简式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种![]() 工程树脂由丙烯腈(
工程树脂由丙烯腈(![]() ,用
,用![]() 表示)、1,
表示)、1,![]() 丁二烯(
丁二烯(![]() ,用
,用![]() 表示)和苯乙烯(
表示)和苯乙烯(![]() ,用
,用![]() 表示)按一定比例共聚而得。
表示)按一定比例共聚而得。
(1)![]() 和
和![]() 三种单体中,
三种单体中,![]() 原子个数比的比值最小的单体是___________(填物质名称)。
原子个数比的比值最小的单体是___________(填物质名称)。
(2)经元素分析可知,该![]() 工程树脂的组成为
工程树脂的组成为![]() (
(![]() 为正整数),则原料中
为正整数),则原料中![]() 和
和![]() 的物质的量之比是____________(用
的物质的量之比是____________(用![]() 表示)。
表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2020年2月,国家卫生健康委办公厅、国家中医药管理局办公室联合发出《关于印发新型冠状病毒肺炎诊疗方案(试行第六版)的通知》。此次诊疗方案抗病毒治疗中增加了阿比多尔这个药物。其中间体I的合成路线如下:

(1)A的结构简式是 _____。
(2)I中含氧官能团名称是_____。
(3)③、⑦的反应类型分别是 _____________、 __________ 。
(4)②的化学方程式为_________________________。
(5)D的同分异构体中,满足下列条件的有_______种。
a. 含有苯环 b.含有-NO2
其中核磁共振氢谱为3组峰,且峰面积之比为1∶2∶6的为____________(任写一种结构简式)。
(6)已知:①当苯环有RCOO-、烃基时,新导入的基团进入原有基团的邻位或对位;原有基团为-COOH时,新导入的基团进入原有基团的间位。②苯酚、苯胺(![]() )易氧化。设计以
)易氧化。设计以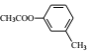 为原料制备
为原料制备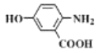 的合成路线(无机试剂任用)__________________。
的合成路线(无机试剂任用)__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气作为清洁能源有着广泛的应用前景,采用天然气制备氢气的流程如下。
![]()
请回答下列问题:
Ⅰ.蒸汽转化:在催化剂的作用下,水蒸气将CH4氧化,结合图表信息回答问题。
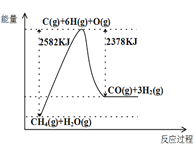
(1)该过程的热化学方程式是__________。
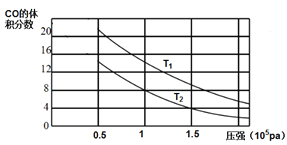
(2)平衡混合物中CO的体积分数与压强的关系如图所示,判断T1和T2的大小关系:T1_______T2(填“>”“<”或“=”),并说明理由__________。
(3)一定温度下,在1L恒容的密闭容器中充入1mol CH4和1mol水蒸气充分反应达平衡后,测得反应前后容器中气体的物质的量之比是3:4,计算该条件下反应的平衡常数为______________。
Ⅱ.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
Ⅲ.模拟H2提纯工艺:将CO2和H2分离得到H2的过程如下:
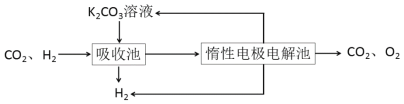
依据图示信息回答:
(4)吸收池中发生反应的离子方程式是_________。
(5)写出电解池中阳极发生的电极反应式________;结合化学用语说明K2CO3溶液再生的原因_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中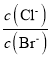 增大
增大
B.在0.1 mol/LCH3COONa溶液中:c(OH﹣)+0.1mol/L>c(CH3COOH)+c(H+)+c(Na+)
C.在10mL 0.1 mol/L的AgNO3溶液中加入6mL等浓度的NaCl溶液,有白色沉淀产生,再加入6 mL等浓度的Na2S溶液,溶液中又有黑色沉淀生成,说明Ksp(Ag2S)< Ksp(AgCl)
D.常温下,10 mL 0.02 mol/L HCl溶液与10 mL 0.02 mol/LBa(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是( )
A. 分子式为C8H8O2的芳香族化合物中属于羧酸的同分异构体有3种
B. 麦芽糖的水解产物有两种,且互为同分异构体
C. 等质量的苯和苯乙烯(![]() )完全燃烧,消耗氧气的体积相同
)完全燃烧,消耗氧气的体积相同
D. 分子式为C4H8Cl2且含有两个甲基的有机物有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胡椒乙酸是合成许多药用生物碱的重要中间体,以苯酚为原料制备胡椒乙酸的合成路线如图所示。

回答下列问题:
(1)下列关于有机物B的说法正确的是 ____________(填字母)。
a.能与FeCl3溶液发生显色反应
b.核磁共振氢谱中只有3组峰
c.能发生银镜反应
d.能与溴水发生加成反应
(2)C的名称是___________,C D的反应类型是_______。
(3)胡椒乙酸(E)中所含官能团的名称为 __________ 。
(4)G生成F的化学方程式为_____________。
(5)W是E的同分异构体,0.5 mol W与足量碳酸氢钠溶液反应生成1 mol C02,已知W的苯环上只有2个取代基,则W的结构共有__________(不含立体异构)种,其中核磁共振氢谱有五组峰的结构简式为_______。
(6)参照上述合成路线,写出以一氯甲苯(![]() )为原料(无机试剂任选)制备苯乙酸的合成路线:____________________
)为原料(无机试剂任选)制备苯乙酸的合成路线:____________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com