
分析 根据m=nM计算碳酸钠质量,每个碳酸钠化学式电离出两个钠离子,则n(Na+)=2n( Na2CO3),根据N=nNA计算钠离子个数;根据C原子守恒知,n(CO32-)=n( Na2CO3).
解答 解:m( Na2CO3)=n( Na2CO3)M( Na2CO3)=1.5mol×106g/mol=159g,每个碳酸钠化学式电离出两个钠离子,则n(Na+)=2n( Na2CO3)=2×1.5mol=3mol,N(Na+)=n(Na+)NA=3mol×NA/mol=3NA;根据C原子守恒知,n(CO32-)=n( Na2CO3)=1.5mol,
故答案为:159;3NA;1.5.
点评 本题考查物质的量有关计算,为高频考点,明确各个物理量之间关系是解本题关键,还可以利用原子守恒分析解答,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | pH值增大 | B. | 水电离出的c(H+)减小 | ||
| C. | c(OH-)增大 | D. | c(H+)•c(OH-)的值增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 50mL 2mol•L-1CaCl2溶液 | B. | 100mL 2mol•L-1NaCl溶液 | ||
| C. | 50mL 4mol•L-1CaCl2溶液 | D. | 100mL 4mol•L-1NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
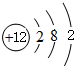 ;画出BC2的电子式
;画出BC2的电子式 ,结构式O=C=O,其晶体类型为分子晶体
,结构式O=C=O,其晶体类型为分子晶体 ,其晶体类型为离子晶体.
,其晶体类型为离子晶体.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{22.4m}{n}$ | B. | $\frac{22400m}{n}$ | C. | $\frac{22400n}{m}$ | D. | $\frac{n}{22.4m}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 在273K(即0℃)时,向如图所示的真空密闭容器A中充入0.5g H2时,测得容器内的压强为1.01×105Pa.由此可以判断A容器的体积约为5.6L.若向A中充入的是O2,压强也是1.01×105pa,则充入的O2质量是8g,若向A容器中充入的是C0气体,使容器内压强达到3.03×105Pa.则充入C0气体的质量是21g.
在273K(即0℃)时,向如图所示的真空密闭容器A中充入0.5g H2时,测得容器内的压强为1.01×105Pa.由此可以判断A容器的体积约为5.6L.若向A中充入的是O2,压强也是1.01×105pa,则充入的O2质量是8g,若向A容器中充入的是C0气体,使容器内压强达到3.03×105Pa.则充入C0气体的质量是21g.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 15种 | B. | 28种 | C. | 32种 | D. | 40种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com