
【题目】某课外小组同学设计如图实验装置(部分夹持仪器未画出)探究氨气的还原性并检验部分产物。
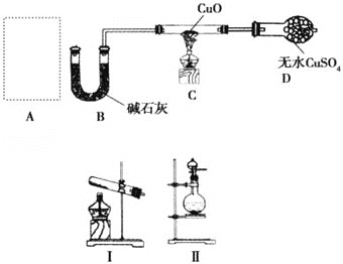
(1)若A中使用装置Ⅰ制取氨气,则化学方程式为__,发生装置试管口略向下倾斜的原因_____;若A中使用装置Ⅱ制取氨气,则分液漏斗中的试剂为__,圆底烧瓶中的固体可以为__。
(2)B中碱石灰的作用是__。
(3)氨气还原炽热氧化铜的化学方程式为__,装置C中的实验现象为__,装置D中的实验现象为__。
(4)①该装置存在明显的缺陷是__。
②请画出改进后需要增加连接的实验装置图________。
【答案】 2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O 防止水倒流使试管炸裂 浓氨水 NaOH(或CaO或碱石灰) 吸收氨气中的水蒸气 3CuO+2NH3
CaCl2+2NH3↑+2H2O 防止水倒流使试管炸裂 浓氨水 NaOH(或CaO或碱石灰) 吸收氨气中的水蒸气 3CuO+2NH3![]() 3Cu+N2+3H2O 黑色CuO变为红色 白色无水CuSO4粉末变蓝 没有尾气吸收装置,NH3排入大气,污染环境
3Cu+N2+3H2O 黑色CuO变为红色 白色无水CuSO4粉末变蓝 没有尾气吸收装置,NH3排入大气,污染环境 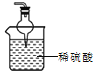
【解析】(1)装置I适用于固体+固体![]() 气体,使用装置I制NH3的反应原理为2NH4Cl+Ca(OH)2
气体,使用装置I制NH3的反应原理为2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O。装置II适用于固体+液体→气体,使用装置II制NH3可用浓氨水与NaOH(或CaO或碱石灰)。
CaCl2+2NH3↑+2H2O。装置II适用于固体+液体→气体,使用装置II制NH3可用浓氨水与NaOH(或CaO或碱石灰)。
(2)B中碱石灰的作用是:吸收氨气中的水蒸气。
(3)氨气与炽热的CuO反应生成N2、Cu和H2O。
(4)①NH3污染大气,该装置的明显缺陷是:没有尾气吸收装置。
②改进方法是:在装置末端增加尾气吸收装置,用稀硫酸吸收NH3并防倒吸。
(1)装置I适用于固体+固体![]() 气体,使用装置I制NH3的反应原理为2NH4Cl+Ca(OH)2
气体,使用装置I制NH3的反应原理为2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O,发生装置试管口略向下倾斜的原因是:防止水倒流使试管炸裂。装置II适用于固体+液体→气体,使用装置II制NH3可用浓氨水与NaOH(或CaO或碱石灰),分液漏斗中的试剂为浓氨水,圆底烧瓶中的固体可以为NaOH(或CaO或碱石灰)。
CaCl2+2NH3↑+2H2O,发生装置试管口略向下倾斜的原因是:防止水倒流使试管炸裂。装置II适用于固体+液体→气体,使用装置II制NH3可用浓氨水与NaOH(或CaO或碱石灰),分液漏斗中的试剂为浓氨水,圆底烧瓶中的固体可以为NaOH(或CaO或碱石灰)。
(2)实验室制得的NH3中都混有H2O(g),B中碱石灰的作用是:吸收氨气中的水蒸气,防止干扰CuO与NH3反应的生成物H2O的检验。
(3)氨气与炽热的CuO反应生成N2、Cu和H2O,反应的化学方程式为3CuO+2NH3![]() 3Cu+N2+3H2O。装置C中的实验现象为:黑色CuO变为红色。由于有H2O生成,装置D中的实验现象为:白色无水CuSO4粉末变蓝。
3Cu+N2+3H2O。装置C中的实验现象为:黑色CuO变为红色。由于有H2O生成,装置D中的实验现象为:白色无水CuSO4粉末变蓝。
(4)①NH3污染大气,该装置的明显缺陷是:没有尾气吸收装置,NH3排入大气,污染环境。
②改进方法是:在装置末端增加尾气吸收装置,用稀硫酸吸收NH3并防倒吸,连接的实验装置图为 。
。


科目:高中化学 来源: 题型:
【题目】环境中氮氧化物的合理控制和治理是减少雾霾天气、优化生存环境的有效途径之一.请运用化学反应原理知识,回答下列问题:.
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染.已知: ①CH4 (g)+4NO2 (g)═4NO(g)+CO2 (g)+2H2O(1)△H1=﹣662kJmol﹣1
②CH4 (g)+4NO(g)═2N2 (g)+CO2 (g)+2H2O(1)△H2=﹣1251kJmol﹣1
据此,写出CH4将NO2还原为N2的热化学方程式:
(2)用活性炭还原法也可处理氮氧化物.有关反应为:C(s)+2NO(g)N2 (g)+CO2 (g)某研究小组向一个容积(3L)恒定的真空密闭容器中加人0.3mol NO和足量的活性炭与催化剂(固体试样的体积忽略不计),在恒温(T1℃)条件下发生反应,经10min反应达到平衡,测得N2的物质的量为0.09mol. ①0min~10min内以v(NO)表示的平均化学反应速率为 .
②下列各项能判断该反应达到平衡状态的是 .
A.容器内压强保持不变
B.速率关系:2v(NO)(正)=v (N2)(逆)
C.容器内CO2的体积分数不变
D.混合气体的密度保持不变
③在相同条件下,若在容器中放人生石灰,则NO的平衡转化率(填“增大”、“不变”或“减小”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH3-CH=CH-COOH,该有机物能发生的反应是( )
①取代反应 ②加成反应 ③使溴水褪色 ④使酸性KMnO4溶液褪色 ⑤酯化反应 ⑥聚合反应
A.以上反应均可发生B.只有⑤不能发生C.只有⑥不能发生D.只有②不能发生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是

A. 正极反应为AgCl +e-=Ag +Cl-
B. 放电时,交换膜右侧溶液中有大量白色沉淀生成
C. 若用NaCl溶液代替盐酸,则电池总反应随之改变
D. 当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:正四面体形分子E和直线形分子G反应,生成四面体形分子L和直线形分子M(组成E分子的元素的原子序数均小于10,组成G分子的元素为第三周期元素)。下列判断中正确的是( )
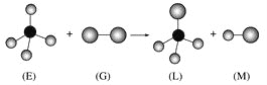
A. 常温常压下,L是一种液态有机物
B. E的二溴代物只有两种结构
C. G具有强氧化性和漂白性
D. 上述反应的类型是取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关催化剂的催化机理等问题可从“乙醇催化氧化实验”得到一些认识,其实验装置如图所示。其实验操作为预先使棉花团浸透乙醇,并按照图示安装好装置;在铜丝的中间部分加热,片刻后开始(间歇性)鼓入空气,即可观察到明显的实验现象。

请回答以下问题:
(1)被加热的铜丝处发生反应的化学方程式为________________________________。
(2)从A管中可观察到____________的实验现象。从中可认识到在该实验过程中,催化剂参加了化学反应,还可认识到催化剂起催化作用时需要一定的_______________________。
(3)实验一段时间后,如果撤掉酒精灯,反应还能否继续进行?__________,原受热部分的铜丝有什么现象?____________,产生这种现象是因为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A,B两种液态有机物均由碳、氢、氧三种元素组成。A能溶于水,它的相对分子质量是60,分子中有8个原子,其中氧原子数与碳原子数相等,且A与碳酸钠溶液混合时冒气泡。B分子中有9个原子,分子内所有原子的核电荷数之和为26,且B只能跟钠反应放出氢气,不能与碳酸钠溶液反应。
(1)A的结构简式为 __________________ ,B的结构简式为 ________________。
(2)写出A与碳酸钠溶液反应的化学方程式________________________________。
(3)写出B与钠反应的化学方程式_____________________________。
(4)写出A与B反应的化学方程式_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性, r溶液是一种常见的强酸,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是

A. 原子半径的大小W<X<Y
B. 元素的非金属性Z>X>Y
C. Y的氢化物常温常压下为液态
D. X的最高价氧化物的水化物为强酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com