
 ��ע��R�������������Ҳ������Hԭ�ӣ�
��ע��R�������������Ҳ������Hԭ�ӣ� ����һ������ɽ�����ϣ��ο�������Ϣ������Ҵ��Ʊ�������ĺϳ�·��
����һ������ɽ�����ϣ��ο�������Ϣ������Ҵ��Ʊ�������ĺϳ�·��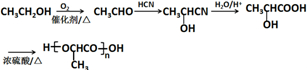 ����ʾ������Ӧ����X$\stackrel{��Ӧ����1}{��}$Y$\stackrel{��Ӧ����2}{��}$Z ����
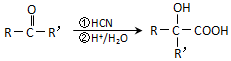
����ʾ������Ӧ����X$\stackrel{��Ӧ����1}{��}$Y$\stackrel{��Ӧ����2}{��}$Z ���� ���� F�����Ӿ۷�Ӧ�����л���������F�ṹ��ʽΪCH2=C��CH3��COOCH3��E�ͼ״�����������Ӧ����F��E�ṹ��ʽΪCH2=C��CH3��COOH��
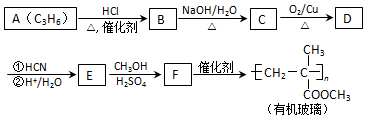
A������������A����ʽ֪��A�ṹ��ʽΪCH2=CHCH3��A��HCl�����ӳɷ�Ӧ����B��B����ȡ����Ӧ����C��C������������Ӧ����D���˴Ź������ױ���Dֻ��һ�ֻ�ѧ�������⣬��D�ṹ��ʽΪCH3COCH3��C�ṹ��ʽΪCH3CH��OH��CH3��B�ṹ��ʽΪCH3CHClCH3��D�����ӳɷ�ӦȻ���ữ�õ�E��
��6�����Ҵ�Ϊ��ʼԭ���Ʊ�������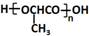 ���Ҵ�������������ȩ����ȩ��HCN�����ӳɷ�Ӧ��Ȼ��ˮ���������ᣬ�����Ӿ۷�Ӧ�����ɾ����ᣮ
���Ҵ�������������ȩ����ȩ��HCN�����ӳɷ�Ӧ��Ȼ��ˮ���������ᣬ�����Ӿ۷�Ӧ�����ɾ����ᣮ
��� �⣺F�����Ӿ۷�Ӧ�����л���������F�ṹ��ʽΪCH2=C��CH3��COOCH3��E�ͼ״�����������Ӧ����F��E�ṹ��ʽΪCH2=C��CH3��COOH��
A������������A����ʽ֪��A�ṹ��ʽΪCH2=CHCH3��A��HCl�����ӳɷ�Ӧ����B��B����ȡ����Ӧ����C��C������������Ӧ����D���˴Ź������ױ���Dֻ��һ�ֻ�ѧ�������⣬��D�ṹ��ʽΪCH3COCH3��C�ṹ��ʽΪCH3CH��OH��CH3��B�ṹ��ʽΪCH3CHClCH3��D�����ӳɷ�ӦȻ���ữ�õ�E��
��1��A�Ľṹ��ʽΪCH2=CHCH3��A����B�ķ�Ӧ����Ϊ�ӳɷ�Ӧ��
�ʴ�Ϊ��CH2=CHCH3���ӳɷ�Ӧ��
��2��C�ṹ��ʽΪCH3CH��OH��CH3��B�ṹ��ʽΪCH3CHClCH3��B����C�Ļ�ѧ����ʽΪCH3CHClCH3+NaOH$\stackrel{H_{2}O}{��}$CH3CH��OH��CH3+NaCl��
�ʴ�Ϊ��CH3CHClCH3+NaOH$\stackrel{H_{2}O}{��}$CH3CH��OH��CH3+NaCl��
��3��D�Ľṹ��ʽΪCH3COCH3�������������6��ԭ�ӹ�ƽ�棬
�ʴ�Ϊ��CH3COCH3��6��
��4��E�ṹ��ʽΪCH2=C��CH3��COOH��E�Ļ�ѧ����Ϊ2-��2-��ϩ�ᣬ
�ʴ�Ϊ��2-��2-��ϩ�
��5��F�ṹ��ʽΪCH2=C��CH3��COOCH3��F��ͬ���칹������ͬʱ��������������
�����뱥��NaHCO3��Һ��Ӧ�������壬˵�������Ȼ���
����ʹBr2�����Ȼ�̼��Һ��ɫ˵������̼̼˫����ȥ���Ȼ��������ĸ�̼ԭ�ӣ������˫�����ĸ�̼��ֱ����2�֣��ֱ����Ȼ�ȡ����Ӧ��6�ֽṹ�������⣻���˫�����ĸ�̼��CH2=C��CH3��2�����Ȼ�ȡ����Ӧ��2�ֽṹ�������⣬����8�ֽṹ�������⣻
���к˴Ź���������ʾΪ4��壬�ҷ������Ϊ3�s2�s2�s1����CH2=C��CH3��CH2COOH��
�ʴ�Ϊ��8��CH2=C��CH3��CH2COOH��
��6�����Ҵ�Ϊ��ʼԭ���Ʊ�������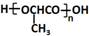 ���Ҵ�������������ȩ����ȩ��HCN�����ӳɷ�Ӧ��Ȼ��ˮ���������ᣬ�����Ӿ۷�Ӧ�����ɾ����ᣬ����Ϊ
���Ҵ�������������ȩ����ȩ��HCN�����ӳɷ�Ӧ��Ȼ��ˮ���������ᣬ�����Ӿ۷�Ӧ�����ɾ����ᣬ����Ϊ ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л�����ƶ���ϳɣ�Ϊ��Ƶ���㣬������ѧ���ķ��������Ŀ��飬��Ҫѧ���Ը��跴Ӧ��Ϣ���ã��ϺõĿ���ѧ������ѧ���Ķ����������ȵ����ͣ��ѵ��Ǻϳ�·����Ƽ���ϢǨ��������������ã���Ŀ�Ѷ��еȣ�


 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 mol CO2��������44g | |
| B�� | 17 g NH3�������22.4 L | |
| C�� | 100 mL 1 mol/L NaOH��Һ�к���1 mol OH- | |
| D�� | ��״���£�11.2 L O2�к���6.02��1023�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe��NO3��3��Һ�м�������HI��Һ��2Fe3++2I-�T2Fe2++I2 | |
| B�� | ��H2O2��H2SO4�Ļ����Һʴ��ͭ��Cu+H2O2+2H+�TCu2++2H2O | |
| C�� | NH4HCO3��Һ�м�����������ʯ��ˮ��Ca2++HCO3-+OH-�TCaCO3��+H2O | |
| D�� | C12ͨ��NaOH��Һ��Cl2+OH-�TCl-+ClO-+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����������ܲ������������ | |
| B�� | �ؽ������Ӷ������Σ����Ҫ����ɵ����ʵı��� | |
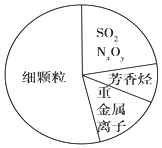
| C�� | SO2��NxOy���������������� | |
| D�� | ��APEC������2014���µ�����ʻ㣬����2014��APEC�����ڼ䱱����������գ�˵������ʵʩ��·���к���Ⱦ��ҵͣ���ȴ�ʩ���ɶž������ķ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
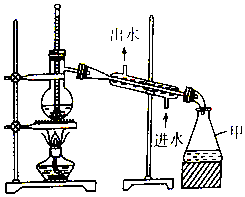
| A�� | ����������ƿ����ֱ���þƾ��Ƽ��� | |
| B�� | �¶ȼ�ˮ����Ӧ������������ƿ֧�ܿڴ� | |
| C�� | ֱ�������ܿ������������ܴ��� | |
| D�� | ʯ������ʱ�ӷ�ʯ��������ˮʱ���üӷ�ʯ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ�Ӱ뾶�Ĵ�С��Z��X��Y | |
| B�� | Z���⻯��ķе�һ����X �ĵ� | |
| C�� | W������������Ӧˮ�����������ͬ��������ǿ | |
| D�� | Y�ĵ�����Z��X�γɵĻ����ﷴӦ��ұ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
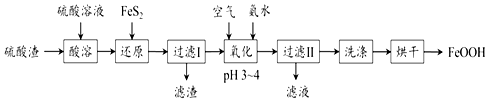
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com