
����Ŀ�����ӣ�Ni��Cd���ɳ�������ִ��������й㷺Ӧ�ã���֪ij���ӵ�صĵ������ҺΪKOH��Һ����䡢�ŵ簴��ʽ���У�Cd+2NiOOH+2H2O ![]() Cd��OH��2+2Ni��OH��2 �� �йظõ�ص�˵����ȷ���ǣ� ��
Cd��OH��2+2Ni��OH��2 �� �йظõ�ص�˵����ȷ���ǣ� ��
A.���ʱ������Ӧ��Ni��OH��2��e��+OH���TNiOOH+H2O
B.�������ǻ�ѧ��ת��Ϊ���ܵĹ���
C.�ŵ�ʱ����������Һ�ļ��Բ���
D.�ŵ�ʱ�������Һ�е�OH���������ƶ�
���𰸡�A
���������⣺A�����ʱ����װ���ǵ��أ������ϵ缫��ӦʽΪ��Ni��OH��2��e��+OH���TNiOOH+H2O����A��ȷ�� B��������ʵ�����ǰѵ���ת��Ϊ��ѧ�ܵĹ��̣���B����
C���ŵ�ʱ�������ϵ缫��ӦʽΪ��Cd��2e��+2OH��=Cd��OH��2 �� ���Լ��Լ�������C����
D���ŵ�ʱ���������Һ���������������ƶ�����D����
��ѡA��
�ŵ�ʱ�����Ϸ����ĵ缫��ӦʽΪ��Cd��2e��+2OH��=Cd��OH��2 �� �����Ϸ����ĵ缫��ӦʽΪ��NiOOH+e��+H2O�TNi��OH��2+OH�� �� ���ʱ�����Ϸ����ĵ缫��ӦʽΪ��Ni��OH��2+OH����e����NiOOH+H2O�������Ϸ����ĵ缫��ӦʽΪ��Cd��OH��2+2e���TCd+2OH�� �� �ŵ�ʱ����Һ���������������ƶ��������ǰѵ���ת��Ϊ��ѧ�ܵ�װ�ã�


 ����������������ϵ�д�
����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и����ڵ����ӣ�����Һ�в��ܴ���������� �� ��
A. Mg2+ K+ NO3- Cl- B. K+ Na+ Mg2+ SO42-
C. H+ SO42- Ba2+ NO3- D. Ca2+ H+ NO3- Cl-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧϰС����������װ�ý��н���CO2�뱥��Na2CO3��Һ��Ӧ�Ʊ�NaHCO3ʵ�飮
��1��ѡȡ��Ҫ��ʵ��װ�ã���ȷ������˳��Ϊ������ţ���
��2��Ϊȷ���ƵõĹ�����Ʒ�Ǵ�����NaHCO3 С��ͬѧ�������ʵ�鷽��������������Ʒ��Һ�뱥�ͳ���ʯ��ˮ��Ӧ���۲�����
�ҷ���������Ʒ��Һ��BaCl2�۲�����
���������ⶨpH��
�����������ط�����
������������������������
��Ϊ�ж��ҷ����Ŀ����ԣ�ijͬѧ�÷�������NaHCO3���Ƶ���Һ����BaCl2��Һ�������Ͻ���ʵ�飬������£� 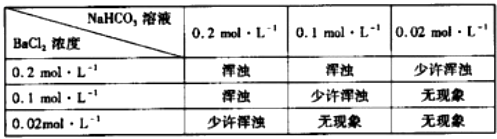
��i����ʵ���ȿ�˵���ҷ����Dz����еģ������������ݣ���ͨ������˵���������ǵ�ԭ�� �� [��֪��0.1 molL��1 NaHC03��Һ�������c��CO32����Ϊ0.0011 molL��1 �� Ksp��BaCO3��=5.1��10��9]
�������������ǵ����ӷ���ʽΪ ��
��ʹ��pH�ƽ��вⶨ�ı������� ��
�ܽ��ж�����ʵ�飬�����Ʒ�ڲ�ͬ���������µ�������������ͼ������գ�
��i����Ʒ�Ĵ���Ϊ ��
�������������ʶ�ʵ��������нϴ����н�С����û�С���Ӱ�죮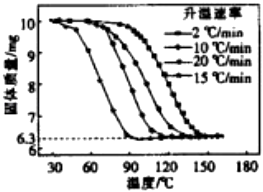
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���2L���ܱ������г���2molPCl3��g����1molCl2��g����������Ӧ��PCl3��g��+Cl2��g��PCl5��g����5min��ƽ�⣬�����е�ѹǿΪ��ʼʱ�� ![]() �����ҷų�37.2kJ����������ش��������⣺
�����ҷų�37.2kJ����������ش��������⣺
��1��ǰ5min�ڣ�v��Cl2��=molL��1min�����¶��£�ƽ�ⳣ��K= ��
��2�������ĸ�ͼ������ȷ˵��������Ӧ�ڽ��е�t1ʱ��ʱ���ﵽƽ��״̬ �� 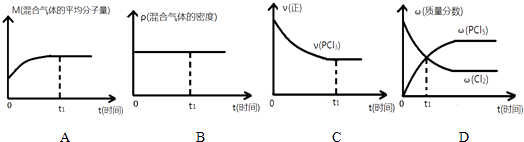
��3��ƽ�������������0.4molPCl3 �� 0.2molCl2��0.2molPCl5 �� ��ƽ����������ƶ����������ƶ������ƶ�������c��PCl3�����������С�����䡱����
��4����ͬ�����£�����ʼʱ����2L���ܱ������г���1molPCl3��g����1molPCl5��g������Ӧ��ƽ������������� kJ��������
��5��PCl5��������ˮ����ȫ��Ӧ����H3PO4��HCl������Ӧ��Ļ��Һ��μ��뵽������Na2CO3��Һ�У���д�����ܷ�����Ӧ�����ӷ���ʽ �� ����֪��H3PO4�ĵ���ƽ�ⳣ����Ka1=7.52��10��3 �� Ka2=6.23��10��8 �� Ka3=2.2��10��13��H2CO3�ĵ���ƽ�ⳣ����Ka1=4.3��10��7 �� Ka2=5.61��10��11��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��PX���л���A��Ӣ����д���ǻ��������зdz���Ҫ��ԭ��֮һ���������������ϡ�������ά����Ĥ��ҩ��ȣ����о���������������ʺϳ�ijҩ���ϳ�·�����£����ַ�Ӧ�Լ����������ԣ���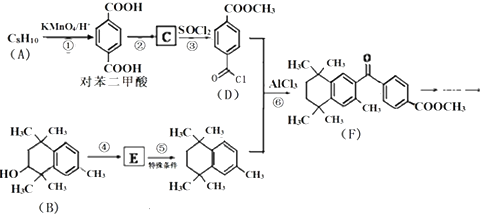
��֪���� ![]()
![]()
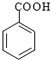
��RCOOH ![]()
![]()
�Իش��������⣺
��1��PX��ԭ��A�Ľṹ��ʽΪ ��
��2��F�����к��������ŵ�����Ϊ�� ��
��3����Ӧ�١��������ķ�Ӧ���ͷֱ�Ϊ�� ��
��4����Ӧ�ܵĻ�ѧ����ʽΪ ��
��5��G�ǶԱ��������ͬϵ��������ȶԱ��������14��G�ж���ͬ���칹�壬��ͬʱ��������������ͬ���칹�����֣�
a�����ڷ����廯���� b������NaHCO3��Һ��Ӧ��������c���ܷ���ˮ�ⷴӦ��������Ӧ
��6����A����ϩΪԭ�Ͽ��Ժϳ�Ŀǰ�����ϲ�����ߵĺϳ���ά����������ά���۶Ա��������Ҷ����������ϳ�·�����£�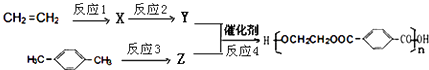
��Ӧ3���Լ�Ϊ ��
��Ӧ2�ͷ�Ӧ4�Ļ�ѧ����ʽ�ֱ�Ϊ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ڻ�������ϵĸ߶�һ���Ա����ڣ� ����
��������������Ҫ��ѧԪ�ص��������һ�� �ڸ�������ĺ��ᶼ��ͬ
�۹��ɺ���ļ������ͬ �ܸ�������ĵ����ʶ���ͬ
�ݹ��ɵ����ʵİ����ᶼ��ͬ
A���٢ڢ� B���٢ڢ� C���ۢܢ� D���٢ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£����淴ӦX��g��+3Y��g��2Z��g������X��Y��Z��ʼŨ�ȷֱ�Ϊc1��c2��c3������Ϊ0����λmol/L��������ƽ��ʱX��Y��Z��Ũ�ȷֱ�Ϊ0.1mol/L��0.3mol/L��0.08mol/L���������жϲ��������ǣ� ��
A.c1��c2=1��3
B.ƽ��ʱ��Y��Z����������֮��Ϊ3��2
C.X��Y��ת���ʲ����
D.c1��ȡֵ��ΧΪ0��c1��0.14mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��CH4��g��+2O2��g��=CO2��g��+2H2O��g����H=��Q1�� 2H2��g��+O2��g��=2H2O��g����H=��Q2��
H2O��g��=H2O��l����H=��Q3
�����£�ȡ�����Ϊ4��1�ļ����H2�Ļ������112L����״���£�������ȫȼ�պ�ָ������£���ų�������Ϊ�� ��
A.4Q1+0.5Q2
B.4Q1+Q2+10Q3
C.4Q1+2Q2
D.4Q1+0.5Q2+9Q3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ɫ��ѧ��ʵ�����߽����ã�����������������ɫ��ѧ������

��ʵ�����ռ���������ͼ����ʾװ��
��ʵ���������������Ƶķ�Ӧʵ��ʱ����ͼ����ʾװ��
��ʵ�������ò������ֱ�պȡŨ�����Ũ��ˮ����������������ε�ʵ��
��ʵ�����в���ͼ����ʾװ�ý���ͭ��ϡ����ķ�Ӧ
A. �ڢۢ�
B. �٢ڢ�
C. �٢ڢ�
D. �٢ۢ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com