
| Y | V | |||
| X | W |
| A. | 原子半径:X>W>V>Y | |
| B. | Y的最高价氧化物的电子式为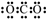 | |
| C. | X的最高价氧化物能与V、W最高价氧化物对应的水化物反应 | |
| D. | 甲、乙混合时所生成的物质为离子化合物,既含有离子键又含有非极性键 |
分析 V、W、X、Y均是元素周期表中短周期元素,V的最简单氢化物为甲,W的最简单氢化物为乙,甲、乙混合时有白烟生成,则V为N,甲为氨气,W为Cl,乙为HCl,Y为C,X为Al,结合元素周期律及元素化合物知识来解答.
解答 解:V、W、X、Y均是元素周期表中短周期元素,V的最简单氢化物为甲,W的最简单氢化物为乙,甲、乙混合时有白烟生成,则V为N,甲为氨气,W为Cl,乙为HCl,Y为C,X为Al,
A.电子层越多,原子半径越大;同周期原子序数大的原子半径小,则原子半径:X>W>Y>V,故A错误;
B.Y的最高价氧化物为二氧化碳,其电子式为 ,故B错误;
,故B错误;
C.X的最高价氧化物为氧化铝,具有两性,能与V、W最高价氧化物对应的水化物(硝酸、高氯酸)反应,故C正确;
D.甲、乙混合时所生成的物质为离子化合物为氯化铵,既含有离子键又含有N-H极性键,故D错误;
故选C.
点评 本题考查位置、结构与性质的综合应用,为高频考点,把握元素的位置、性质、元素周期律等为解答的关键,侧重分析与应用能力的考查,注意元素化合物及化学键,题目难度不大.


 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:推断题
| 族 周期 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 压强/Mpa C% 温度/℃ | 0.1 | 10 | 20 |
| 200 | 15.3 | 81.5 | 86.4 |
| 300 | 2.2 | a | 64.2 |
| 400 | 0.4 | 25.1 | 38.2 |
| 500 | 0.1 | 10.6 | 19.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
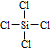 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 以葡萄糖为燃料的微生物燃料电池结构示意图如图所示. 关于该电池的叙述不正确的是( )
以葡萄糖为燃料的微生物燃料电池结构示意图如图所示. 关于该电池的叙述不正确的是( )| A. | 该电池不能在高温下工作 | |
| B. | 电池右侧电极反应为:C6H12O6+6H2O-24e-=6CO2↑+24H+ | |
| C. | 放电过程中,H+通过质子交换膜向电池右侧迁移 | |
| D. | 在电池反应中,每消耗1mol氧气,理论上能生成CO2 22.4 L(标况) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将得到的m g固体放到氧气中充分灼烧后,固体质量变为4.8 g | |
| B. | 生成的CO2已被Ba(OH)2溶液完全吸收,Ba2+沉淀完全 | |
| C. | Ba(OH)2溶液吸收CO2后的溶液中有BaCO3和Ba(HCO3)2,且物质的量的比为2:1 | |
| D. | 原混合物中CuO与Fe2O3的质量比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
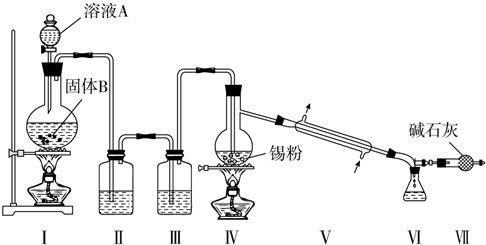
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com