
【题目】苯乙烯是工业上是合成树脂、离子交换树脂及合成橡胶等的重要单体,工业上可用乙苯催化脱氢方法制备苯乙烯:![]() (g)
(g)![]() (g)+H2(g) △H=+QkJ·mol-1
(g)+H2(g) △H=+QkJ·mol-1
请回答下列问题:
(1)已知乙苯(g)、苯乙烯(g)的燃烧热分别为a kJ·mol-1、bkJ·mol-1,则氢气的燃烧热为_____kJ·mol-1(用含有Q、b、c的表达式表示,其中Q、b、c均大于0)。
(2)673 K时,在一恒容密闭容器中充入5 mol乙苯(g),反应达到平衡后容器内气体的压强为p1;若再充入amol的乙苯(g),重新达到平衡后容器内气体的压强为2p1,则a____________5。
(3)在实际生产中,在恒压条件下常以高温水蒸气作为反应体系的稀释剂(水蒸气不参加反应),此时乙苯的平衡转化率与水蒸气的用量、压强(p)的关系如图所示。
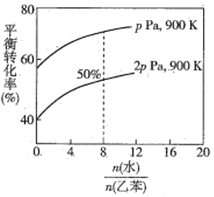
①加入水蒸气稀释剂能提高乙苯转化率的原因是________________________________。
②在实际生产过程中,当控制反应温度为900 K时生产效率最佳,选用此温度进行生产的原因为________ (答两点)。
③用平衡分压代替平衡浓度计算,其中,分压=总压×物质的量分数,则900K时的平衡常数Kp=_______。
④改变下列条件,能使乙苯的反应速率和转化率一定增大的是________ (填标号)。
A.恒容时加入稀释剂水蒸气 B.压强不变下,温度升至1500 K
C.在容积和温度不变下充入Ar D.选用催化效果更好的催化剂
(4)已知苯乙烯可催化氧化生成苯乙醛: ![]() (g) + 2O2→
(g) + 2O2→![]() + CO2 + H2O,若把该反应设计为酸性燃料电池,则电池负极的电极反应式为___________________,若该电池消耗标准状况下11.2 L的O2,则外电路中理论上应转移电子的物质的量为________ mol。
+ CO2 + H2O,若把该反应设计为酸性燃料电池,则电池负极的电极反应式为___________________,若该电池消耗标准状况下11.2 L的O2,则外电路中理论上应转移电子的物质的量为________ mol。
【答案】 (Q+a-b) > 保持总压不变,充入水蒸气,容器体积增大,各组分的浓度同倍数减小,利于反应正向进行,乙苯转化率增大(或体系总压强不变时,加入稀释剂,参与反应的各物质浓度同等程度减小,相当于反应体系减压,故平衡向气体物质的量增大的方向移动,乙苯转化率增大) 乙苯转化率较大;催化剂活性较高;反应速率较快(任答以上两点即可) ![]() B
B ![]() -8e-+3H2O=
-8e-+3H2O=![]() +8H++CO2 2
+8H++CO2 2
【解析】(1)工业上可用乙苯催化脱氢方法制备苯乙烯:![]() (g)
(g)![]() (g)+H2(g) △H=+QkJ·mol-1,①
(g)+H2(g) △H=+QkJ·mol-1,①![]() +21/2O2(g)→8CO2(g)+5H2O(l)△H=-akJ·mol-1,②
+21/2O2(g)→8CO2(g)+5H2O(l)△H=-akJ·mol-1,②![]() +10O2(g)→8CO2(g)+4H2O(l)△H=-bkJ·mol-1,③H2(g)+1/2O2(g)→2H2O(l)△H=-xkJ·mol-1,由盖斯定律可知,①-②-③得到
+10O2(g)→8CO2(g)+4H2O(l)△H=-bkJ·mol-1,③H2(g)+1/2O2(g)→2H2O(l)△H=-xkJ·mol-1,由盖斯定律可知,①-②-③得到![]() (g)
(g)![]() (g)+H2(g) △H=+QkJ·mol-1,a-b-x=Q,x= (Q+a-b);(2)恒容密闭容器中,物质的量与压强成正比,673K时,在一恒容密闭容器中充入5mol乙苯(g),反应达到平衡后容器内气体的压强为p1;若再充入amol的乙苯(g),重新达到平衡后容器内气体的压强为2p1,a>5。(3)①加入水蒸气稀释剂能提高乙苯转化率的原因是保持总压不变,充入水蒸气,容器体积增大,各组分的浓度同倍数减小,利于反应正向进行,乙苯转化率增大(或体系总压强不变时,加入稀释剂,参与反应的各物质浓度同等程度减小,相当于反应体系减压,故平衡向气体物质的量增大的方向移动,乙苯转化率增大)。②在实际生产过程中,当控制反应温度为900K时生产效率最佳,选用此温度进行生产的原因为:乙苯转化率较大、催化剂活性较高、反应速率较快(任答以上两点即可)。③取图象上900K,2p,转化率为50%的点,写出三段式,平衡时水为8体积,三种物质各0.5mol,用平衡分压代替平衡浓度计算,其中,分压=总压×物质的量分数,三种物质的分压均为2p×0.5/9.5,则900K时的平衡常数Kp
(g)+H2(g) △H=+QkJ·mol-1,a-b-x=Q,x= (Q+a-b);(2)恒容密闭容器中,物质的量与压强成正比,673K时,在一恒容密闭容器中充入5mol乙苯(g),反应达到平衡后容器内气体的压强为p1;若再充入amol的乙苯(g),重新达到平衡后容器内气体的压强为2p1,a>5。(3)①加入水蒸气稀释剂能提高乙苯转化率的原因是保持总压不变,充入水蒸气,容器体积增大,各组分的浓度同倍数减小,利于反应正向进行,乙苯转化率增大(或体系总压强不变时,加入稀释剂,参与反应的各物质浓度同等程度减小,相当于反应体系减压,故平衡向气体物质的量增大的方向移动,乙苯转化率增大)。②在实际生产过程中,当控制反应温度为900K时生产效率最佳,选用此温度进行生产的原因为:乙苯转化率较大、催化剂活性较高、反应速率较快(任答以上两点即可)。③取图象上900K,2p,转化率为50%的点,写出三段式,平衡时水为8体积,三种物质各0.5mol,用平衡分压代替平衡浓度计算,其中,分压=总压×物质的量分数,三种物质的分压均为2p×0.5/9.5,则900K时的平衡常数Kp
![]() (g)
(g)![]() (g)+H2(g)
(g)+H2(g)
开始 1
变化 0.5 0.5 0.5
平衡 0.5 0.5 0.5
Kp=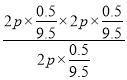 =2p/19
=2p/19
④A.恒容时加入稀释剂水蒸气,乙苯的分压、浓度不变,故A 错误; B.压强不变下,温度升至1500K,反应速率加快,平衡正向移动转化率增大,故B正确;C.在容积和温度不变下充入Ar,乙苯的分压、浓度不变,故C 错误;D.选用催化效果更好的催化剂,也不能使平衡移动,故D错误;故选B。(4)已知苯乙烯可催化氧化生成苯乙醛:![]() (g)+2O2→
(g)+2O2→![]() +CO2/span>+H2O,若把该反应设计为酸性燃料电池,苯乙烯作还原剂,在负极失电子,被氧化在苯乙醛和二氧化碳,则电池负极的电极反应式为.
+CO2/span>+H2O,若把该反应设计为酸性燃料电池,苯乙烯作还原剂,在负极失电子,被氧化在苯乙醛和二氧化碳,则电池负极的电极反应式为. ![]() -8e-+3H2O=
-8e-+3H2O=![]() +8H++CO2,根据反应方程式,每消耗2mol氧气,转移8mol电子,若该电池消耗标准状况下11.2L的O2,则外电路中理论上应转移电子的物质的量为2mol。
+8H++CO2,根据反应方程式,每消耗2mol氧气,转移8mol电子,若该电池消耗标准状况下11.2L的O2,则外电路中理论上应转移电子的物质的量为2mol。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在1200℃时,天然气脱硫工艺中会发生下列反应: H2S(g)+ ![]() O2(g)═SO2(g)+H2O(g)△H1
O2(g)═SO2(g)+H2O(g)△H1
2H2S(g)+SO2(g)═ ![]() S2(g)+2H2O(g)△H2
S2(g)+2H2O(g)△H2
H2S(g)+ ![]() O2(g)═S(g)+H2O(g)△H3
O2(g)═S(g)+H2O(g)△H3
2S(g)═S2(g)△H4
则△H4的正确表达式为( )
A.△H4= ![]() (△H1+△H2﹣3△H3)
(△H1+△H2﹣3△H3)
B.△H4= ![]() (3△H3﹣△H1﹣△H2)
(3△H3﹣△H1﹣△H2)
C.△H4= ![]() (△H1+△H2﹣3△H3)
(△H1+△H2﹣3△H3)
D.△H4= ![]() (△H1﹣△H2﹣3△H3)
(△H1﹣△H2﹣3△H3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、环境等各方面紧密相关,下列相关说法正确的是
A. 机动车单双号限行是从根本上解决汽车尾气污染问题的一种途径
B. 油锅着火应立即用水浇灭
C. 石灰乳刷墙后逐渐变硬的原因是石灰乳在空气中逐渐失水干燥
D. 我们已将PM2.5纳入空气质量检测报告
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列转化关系(反应条件略去),A、B、C、D中均含有同一种元素,回答下头问题:
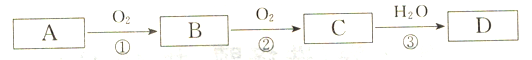
(1)若A为Na,则固体C的颜色为__________________,写出反应③的化学方程式___________________________。
(2)若A为N2,写出反应③的化学方程式___________________________。
(3)若A为S,写出D的浓溶液与Cu在加热情况下反应的化学方程式____________________。
(4)若A为NH3,则__________(填“能”与“不能”)用铁制容器储存D的浓溶液。写出过量Fe与D的稀溶液反应(还原产物只有B)的离子方程式_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)主要用于棉纺、亚麻、腈纶、涤纶等纤维漂白(不适于羊毛、绢丝、粘胶丝、尼龙等),也可用于食品、饮用水消毒、纸张漂白和鱼药制造。工业上常用电解法生产亚氯酸钠(NaClO2),请根据下面的工艺流程图回答下列问题:

已知:纯的ClO2易分解爆炸。一般用稀有气体或空气稀释到10%以下安全。
(1)电解饱和NaCl溶液之前须除去其中的Ca2+、Mg2+、SO42-等杂质,依次加入BaCl2溶液、Na2CO3溶液、NaOH溶液,充分反应后将沉淀一并滤去,若经检测发现滤液中SO42-的浓度仍大于10-5mol·L -1,其可能的原因为____________________,滤液中c(CO32-)∶c(SO42-)为____________。[已知:Ksp(BaSO4 )= 1.0×10 -10,Ksp(BaCO3 )= 5.0×10-9 ]
(2)无隔膜电解槽内发生的反应中氧化产物、还原产物的物质的量之比为____________。
(3)将制得的ClO2 通入电解槽的阴极室,饱和NaCl溶液通入电解槽的阳极室,通电一段时间后可得到产品,电解时阴极的电极反应式为_____________________________。
(4)将ClO2 气体通入含CN-的电镀废水可得到对环境无污染的物质,反应的离子方程式为______________。
(5)ClO2溶液的浓度含量可用碘量法测定,其原理为在盐酸介质中ClO2与I-发生反应:2ClO2+8H++10I-=2Cl-+5I2+4H2O,再用Na2S2O3标准液滴定生成的I2,通过计算即可确定ClO2溶液浓度含量。已知:I2+2Na2S2O3=2NaI+Na2S4O6。
①滴定过程中需要滴加的指示剂为____________。
②取V1 mL的ClO2溶液加入到适量的盐酸和KI溶液中,反应完毕后再用0.lmol·L-1 的Na2S2O3溶液滴定反应后的溶液,若消耗了V2mL的Na2S2O3溶液,则ClO2 的浓度为____________ g·L-1。(杂质不参与反应,ClO2 的还原产物为Cl- )
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在由水电离产生的H+浓度为1×10﹣13molL﹣1的溶液中,一定能大量共存的离子组是( )
A.K+、Cl﹣、NO ![]() 、S2﹣
、S2﹣
B.Na+、Ca2+、Cl﹣、HCO ![]()
C.K+、Ba2+、Cl﹣、NO ![]()
D.SO ![]() 、Mg2+、I﹣、S2O
、Mg2+、I﹣、S2O ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可以用如图所示装置制备、干燥、收集气体的是( )
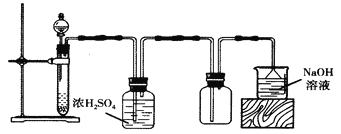
A. 以MnO2、浓盐酸为原料,制备Cl2
B. 以Na2SO3固体、质量分数为70%的浓硫酸为原料,制备SO2
C. 以浓氨水、生石灰为原料,制备NH3
D. 以Cu、稀硝酸为原料,制备NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B两种化合物由M、X两种元素组成,已知A中M元素的质量分数为44.0%,B中M元素的质量分数为34.5%,A的化学式为MX2,则B的化学式为 ( )
A. MX B. M2X3
C. MX3 D. MX4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关1mol O2的说法中,不正确的是(NA表示阿伏伽德罗常数)( )
A.质量为32g
B.含氧原子数为NA
C.含氧分子数为NA
D.在标准状况下,体积约为22.4L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com