
【题目】反应C(s)+H2O(g)![]() CO(g)+H2(g)在一定容积的密闭容器中进行,则下列说法或结论中,能够成立的是( )
CO(g)+H2(g)在一定容积的密闭容器中进行,则下列说法或结论中,能够成立的是( )
A. 其他条件不变仅将容器的体积缩小一半,反应速率减小
B. 保持体积不变,充入少量He气体使体系压强增大,反应速率一定增大
C. 反应达平衡状态时:v(CO)正=v(H2O)逆
D. 其他条件不变,适当增加C(s)的质量会使反应速率增大
科目:高中化学 来源: 题型:
【题目】炽热的炉膛内有反应:![]() 往炉膛内通入水蒸气时,有如下反应:
往炉膛内通入水蒸气时,有如下反应:![]() ,
,![]() ,
,![]() ,其能量变化示意图如下,
,其能量变化示意图如下,
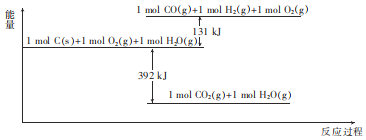
已知CO的燃烧热为![]() 。下列有关说法正确的是
。下列有关说法正确的是![]()
A.![]()
B.![]() 的燃烧热为
的燃烧热为![]()
C.在反应![]() 中,反应物总键能大于生成物总键能
中,反应物总键能大于生成物总键能
D.往炽热的炉膛内通入水蒸气可节省燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知苯乙烯的结构为![]() 。有关该物质的下列说法正确的是( )
。有关该物质的下列说法正确的是( )
A. 该物质在一定条件下和氢气完全加成,加成产物的一溴取代物 6 种
B. 该物质能使溴水和酸性高锰酸钾溶液褪色,褪色原理完全相同
C. 苯乙烯分子的所有原子不可能在同一平面上
D. 除去乙苯中混有的苯乙烯可以通入等量氢气反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知一定温度下,2X(g)+Y(g)![]() mZ(g) ΔH=-a kJ·mol-1(a>0),现有甲、乙两容积相等且固定的密闭容器,在保持该温度恒定的条件下,向密闭容器甲中通入2mol X和1mol Y,达到平衡状态时,放出热量b kJ;向密闭容器乙中通入1mol X和0.5mol Y,达到平衡时,放出热量c kJ,且b>2c,则a、b、m的值或关系正确的是( )
mZ(g) ΔH=-a kJ·mol-1(a>0),现有甲、乙两容积相等且固定的密闭容器,在保持该温度恒定的条件下,向密闭容器甲中通入2mol X和1mol Y,达到平衡状态时,放出热量b kJ;向密闭容器乙中通入1mol X和0.5mol Y,达到平衡时,放出热量c kJ,且b>2c,则a、b、m的值或关系正确的是( )
A.m=4B.a=bC.a<![]() D.m≤2
D.m≤2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌与100mL18.5mol·L-1的浓硫酸充分反应后,锌完全溶解,同时生成气体甲33.6L(标准状况)。将反应后的溶液稀释至1L,测得溶液的c(H+)=0.1mol·L-1。请计算:
(1)反应中共消耗H2SO4的物质的量为__。
(2)反应中共消耗Zn的质量为__。
(3)气体的成分及物质的量之比为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸铝广泛应用在显像管生产,稀土的提炼等,工业上具体流程如下:

已知:①硝酸铝白色透明结晶。易溶于水和乙醇,极微溶于丙酮,几乎不溶于乙酸乙酯。
②熔点73℃,在135℃时分解。
③硝酸和铝反应的还原产物分布如图1。

某兴趣小组在实验室制取硝酸铝,请回答:
(1)从工业生产角度考虑稀硝酸的最佳浓度范围为________ mol·L-1。反应2中的离子方程式____________。
(2)下列说法合理的是________。
A 反应1中加入的NaOH溶液,除油污和氧化膜,所以要足量
B 没有真空,也可在水浴条件下蒸发,防止Al(NO3)3的分解
C Al(NO3)3·9H2O干燥时,可放在如图2的干燥器中,隔板下放上浓硫酸吸水,由于吸附力较大,要用力垂直拉开玻璃盖
D 制取后的Al(NO3)3必须密封保存
(3)Al(NO3)3·9H2O也可以和SOCl2反应,除了生成Al(NO3)3,其它产物都是酸性气体,有关的方程式是______________;
(4)由铝制备Al(NO3)3的装置如图3:
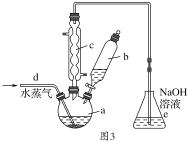
①通入水蒸气的作用是提高温度和________。
②e中很难除尽尾气,理由是_______________, Al(NO3)3·9H2O晶体吸附HNO3,合适的洗涤剂是________。
③有人认为C的冷凝管是多余的,他提供的理由可能是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的气球.关闭K2,将等量且少量的NO2通过K1、K3分别充入A、B中,反应起始时,A、B的体积相同.(已知:2NO2(g) ![]() N2O4(g) ΔH<0)
N2O4(g) ΔH<0)

(1)一段时间后,反应达到平衡,此时A、B中生成N2O4的速率是vA______vB(填“>”、“<”或“=”);若打开活塞K2,气球B将______(填“变大”、“变小”或“不变”).
(2)关闭活塞K2,若在A、B中再充入与初始量相等的NO2,则达到平衡时,NO2的转化率αA将________(填“增大”、“减小”或“不变”);若分别通入等量的氖气,则达到平衡时,A中NO2的转化率将________,B中NO2的转化率将______(填“变大”、“变小”或“不变”).
(3)室温下,若A、B都保持体积不变,将A套上一个绝热层,B与外界可以进行热传递,则达到平衡时,______中的颜色较深.
(4)若在容器A中充入4.6 g的NO2,达到平衡后容器内混合气体的平均相对分子质量为57.5,则平衡时N2O4的物质的量为___________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究Fe(NO3)2等硝酸盐热分解产物和产物的性质,某化学小组开展如下探究:
(查阅资料)2KNO3![]() 2KNO2+O2↑ Fe(NO3)2
2KNO2+O2↑ Fe(NO3)2![]() FexOy+NO2↑+O2↑
FexOy+NO2↑+O2↑
实验一:探究Fe(NO3)2热分解固体产物中铁元素的价态。该小组甲同学将分解后的固体产物溶于足量的稀H2SO4得到相应两份溶液,进行以下探究实验。
(1)(提纯猜想)
猜想一:铁元素只显+2价;
猜想二:铁元素_____________;
猜想三:铁元素既有+2价又有+3价。
(实验操作)①向一份溶液中滴入KSCN溶液;向另一份溶液中滴入酸性KMnO4稀溶液。
(2)(实验现象)实验①_____________________;实验②____________________。
(3)(实验结论)猜想二成立,则Fe(NO3)2分解的化学方程式是_________________。
实验二:
(4)探究Fe(NO3)2热分解气体产物的性质。小组乙同学进行料如下实验,请完成实验空缺部分内容。限选试剂和用品:浓H2SO4溶液、4mol/LNaOH溶液、0.1mol/LBaCl2溶液、带火星的木条、0.1mol/L酸性KMnO4溶液、蒸馏水。
实验步骤 | 预期现象和结论 |
步骤1:取少量Fe(NO3)2固体于试管中,加热分解。 | ____________________________________,说明分解产生的气体中含有NO2。 |
步骤2:将产生的气体依次通过盛有足量_________________、浓硫酸的洗气瓶,______________________在最后一个出口检验。 | _____________________________________,说明分解产生的气体中含O2。 |
实验三:KNO3中混有Fe(NO3)2,为确定其中铁元素的含量,小组丙同学进行如下实验:①取混合物样品10g,充分加热分解;②将固体产物溶解、过滤,取沉淀进行洗涤、干燥,称得其质量为3.2g。则混合物中铁元素的质量分数为__________________。(保留三位有效数字,相对原子质量:Fe:56 O:16)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(s)+3B(g)![]() 2C(g)+D(g)经2 min B的浓度减少0.6 mol·L-1。下列有关说法正确的是
2C(g)+D(g)经2 min B的浓度减少0.6 mol·L-1。下列有关说法正确的是
①用A表示的反应速率是0.4 mol·L-1·min-1
②在2 min末时,反应物B的反应速率是0.3 mol·L-1·min-1
③在这2 min内用C表示的平均速率为0.2 mol·L-1·min-1
④在2 min时,B、C、D的浓度比一定为3∶2∶1
⑤若D的起始浓度为0.1 mol·L-1,则2 min时D的浓度为0.3 mol·L-1
A. ①②③B. ②④C. ④⑤D. ③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com