
分析 发生反应:Ba(OH)2+H2SO4=BaSO4↓+2H2O、2NaOH+H2SO4=Na2SO4+2H2O,当滴至沉淀不再增加时,所消耗的酸的体积是滴定至终点时所消耗酸体积的一半,说明2个反应消耗的H2SO4的体积是一样的,也就是物质的量是一样的,所以Ba(OH)2、NaOH的物质的量浓度比为1:2,而原溶液中2c[Ba(OH)2]+c(NaOH)=0.1mol/L,当滴到沉淀不再增加时:溶液中只有NaOH提供的OH-,根据c(H+)=$\frac{{K}_{W}}{C(O{H}^{-})}$结合pH=-lgc(H+)求解.
解答 解:用0.025mol/LH2SO4滴定,发生反应:Ba(OH)2+H2SO4=BaSO4↓+2H2O、2NaOH+H2SO4=Na2SO4+2H2O,当滴至沉淀不再增加时,所消耗的酸的体积是滴定至终点时所消耗酸体积的一半,说明2个反应消耗的H2SO4的体积是一样的,也就是物质的量是一样的,所以Ba(OH)2、NaOH的物质的量浓度比为1:2,
因为pH=13,pH=-lgc(H+),c(H+)=10-13mol/L,可知c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-13}}$=0.1mol/L,
所以原溶液中2c[Ba(OH)2]+c(NaOH)=0.1mol/L,故2c[Ba(OH)2]+2c[Ba(OH)2]=0.1mol/L,
设c[Ba(OH)2]=x,则c(OH-)=2x,
2x+2x=0.1,解得x=0.025mol/L,即2c[Ba(OH)2]=0.05mol/L,c(NaOH)=0.050mol/L,
从中取出24mL,V1=24mL,c(H2SO4)=0.025mol/L,c(H+)=0.05mol/L,滴定终点所需硫酸的体积:V2=$\frac{0.1×24}{0.05}$mL=48mL,当滴到沉淀不再增加时,所消耗的酸的体积是滴定至终点所耗酸体积的一半为24mL,此时总体积为24mL+24mL=48mL,溶液中只有NaOH提供的OH-,c(OH-)=$\frac{0.05mol/L×24mL}{48mL}$=0.025 mol/L,c(H+)=$\frac{1{0}^{-14}}{0.025}$mol/L=4×10-13 mol/L,pH=-lg4×10-13=12.4,
①由上述计算可知,滴到沉淀不再增加时,溶液的pH为12.4,故答案为:12.4;
②由上述计算可知,原混合溶液中Ba(OH)2物质的量浓度为0.025mol/L,NaOH的物质的量浓度为 0.050mol/L,故答案为:0.025mol/L;0.05mol/L.
点评 本题考查化学方程式的计算,为高频考点,把握信息及方程式确定溶液中氢氧化钡与氢氧化钠物质的量之比为1:2为解答的关键,侧重分析与计算能力的考查,题目难度较大.


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 聚乙烯和乙烯性质相似,都能发生加成反应 | |
| B. | 纤维素、橡胶和光导纤维都属于有机高分子化合物 | |
| C. | 乙烯和乙醇都可发生加成反应 | |
| D. | 等量的CH4和Cl2在光照下反应不能生成纯净的CH3Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度 | B. | 使用催化剂 | C. | 增大H2浓度 | D. | 减小压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
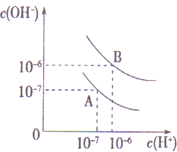 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④⑤ | B. | ②④ | C. | ①③⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
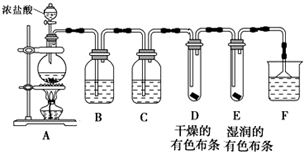
| 实验方法 | 实验现象 | 结论 |
| 分别向A、B溶液中滴加2滴①KSCN溶液 | ②两份溶液都变血红色 | 生成物中都有FeCl3 |
| 分别向A、B溶液中滴加几滴KMnO4溶液 | 两份溶液颜色均无明显变化 | 生成物中都不含③FeCl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com