
 CH3OH(g) ��H��
CH3OH(g) ��H��
| A�����������ƶ� | B�����淽���ƶ� | C������ƽ��״̬ | D�����ж� |
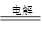 2NaOH+H2��+Cl2��
2NaOH+H2��+Cl2��

 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��SO2�Ĵ�������һ�����ȵķ�Ӧ�������¶ȣ���Ӧ���ʼӿ� |
| B��������ˮΪ֮��������ˮ��˵����ͬ������ˮ�ͱ���ˮ�������ϸ� |
C��A(g)+3B(g)  2C(g)��ƽ����£���ѹ��ƽ�������ƶ���ƽ�ⳣ��Kֵ���� 2C(g)��ƽ����£���ѹ��ƽ�������ƶ���ƽ�ⳣ��Kֵ���� |
| D����KI��Һ�м����Ȼ������壬������ɻ�ɫ��˵��ͬ�¶���Ksp(AgI)< Ksp(AgCl) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������pH��ͬ��KOH��Һ��K2CO3��Һ����ˮ�������c(OH-) |
| B��Ũ�Ⱦ�Ϊ0.1mol��L-1��(NH4)2CO3��Һ��(NH4)2SO4��Һ�е�c(NH4+) |
| C��3 L 0.1 mol��L-1CH3COOH��Һ��1L 0.3 mol��L-1CH3COOH��Һ�е�H+������ |
| D���к�pH���������ͬ��NaOH��Һ�Ͱ�ˮ��������H2SO4�����ʵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ѧ��Ӧ�е������仯������Ϊ�����ı仯 |
| B������������¯�ĸ߶ȿ��Խ���β����CO�ĺ��� |
| C�����ۼ������������Ǽ��븺�������ܴ�����ѧ��Ӧ���� |
| D����ú��������ȼ�տ������ú��ȼ��Ч�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| A�������¶� | B��������� | C����XQ3��ʱ�����ȥ | D������Ӧ��ϵ��ѹǿ |
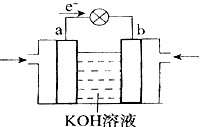
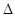 H=��393.5kJ/mol
H=��393.5kJ/mol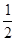 Y2��g��=WY2��g����
Y2��g��=WY2��g����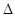 H=��238.0kJ/mol���� 24g W��һ������Y2��Ӧ���ų�����362.5 kJ�����ò���ɷּ����ʵ���֮��Ϊ ��
H=��238.0kJ/mol���� 24g W��һ������Y2��Ӧ���ų�����362.5 kJ�����ò���ɷּ����ʵ���֮��Ϊ ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����ű���ʳ��ˮ�ķ����ռ����� |
| B���ڷ��ڵ�����ˮ�еμ�FeCl3��Һ����Fe(OH)3���� |
| C����FeCl3��Һ�м�AgNO3��Һ��������ɫ���� |
| D����AgCl ��ˮ������Һ�м���������Na2S��Һ������ɫ����ת��Ϊ��ɫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���ⶨ�кͷ�Ӧ�ķ�Ӧ��ʱ����С���ձ���������ֽ�������ǹ̶�С�ձ� |
| B������50mL 0.55mo1��L��1������������Һ���ֱ���50mL 0.50mo1��L��1�������50mL 0.50mo1��L��1�������ַ�Ӧ������Ӧ�ⶨ���кͷ�Ӧ�ķ�Ӧ�Ȳ���� |
| C�����к͵ζ�ʵ���У��ζ���������ˮϴ�Ӻ�Ȼ���ñ�Һ��ϴ���ټӽ���Һ |
| D�������к͵ζ�����ʱ����������ƿ������ת����������Һ�����٣��۾�Ҫʼ��ע�ӵζ�������ҺҺ��ı仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��



| A�����뾶: K��>Cl��>S2��>Na�� | B���ȶ���:HI> HBr>HCl>HF | C������: HClO4>H2SO4>H3PO4>H4SiO4 | D���۵㣺���ʯ��NaCl��SiO2��Na |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com