
| A. | 某同学的体检报告单显示其血液中葡萄糖含量为4.94mmol/L,mmol/L是物质的量的单位 | |
| B. | 石油是复杂的混合物,通过分馏可以获得汽油、煤油等,通过催化重整可以获得乙烯、丙烯等 | |
| C. | 自然界中的方铅矿(PbS),遇上CuSO4溶液会慢慢变成铜蓝(CuS)说明Ksp(PbS)>Ksp(CuS) | |
| D. | 水玻璃是制备木材防火剂的原料,其主要成分是二氧化硅 |
分析 A.mmol/L是物质的量浓度单位;
B.乙烯、丙烯是石油的裂解的产物;
C.结构相同的物质,溶度积常数大的物质能转化为溶度积常数小的物质;
D.水玻璃为硅酸钠的水溶液.
解答 解:A.某同学的体检报告单显示其血液中葡萄糖含量为4.94mmol/L,mmol/L是物质的量浓度单位,故A错误;
B.石油通过裂化可得到乙烯、丙烯,故B错误;
C.结构相同的物质,溶度积常数大的物质能转化为溶度积常数小的物质,所以在CuSO4溶液中加入PbS,可转变为铜蓝(CuS),则Ksp(PbS)>Ksp(CuS),故C正确;
D.水玻璃是制备木材防火剂的原料,其主要成分是硅酸钠的水溶液,故D错误;
故选:C.
点评 本题为综合题,涉及物质的量浓度有关概念、石油的炼制、沉淀的转化、水玻璃的成分及用途,明确石油的炼制方法,熟悉溶度积规则是解题关键,题目难度不大.


科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
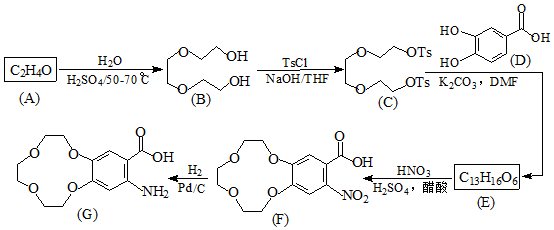
 .
. .
. .
.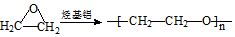 .
.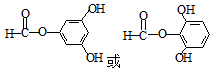 .
.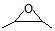 )和邻二苯酚为原料(其它试剂任选),设计制备
)和邻二苯酚为原料(其它试剂任选),设计制备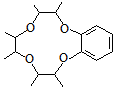 的合成路线.
的合成路线.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
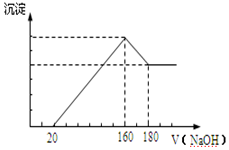
 常温下,在10mL 0.1mol•L-1Na2CO3溶液中逐滴加入0.1mol•L-1HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示(CO2因逸出未画出,忽略因气体逸出引起的溶液体积变化),下列说法正确的是( )
常温下,在10mL 0.1mol•L-1Na2CO3溶液中逐滴加入0.1mol•L-1HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示(CO2因逸出未画出,忽略因气体逸出引起的溶液体积变化),下列说法正确的是( )| A. | 在0.1 mol•L-1Na2CO3溶液中:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) | |
| B. | 当溶液的pH为7时,溶液的总体积为20 mL | |
| C. | 在B点所示的溶液中,离子浓度最大的是HCO3- | |
| D. | 在A点所示的溶液中:c(CO32-)=c(HCO3-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用K2FeO4代替Cl2处理饮用水,既有杀菌消毒作用,又有净水作用 | |
| B. | 古有“青蒿一握,以水二升渍,绞取汁”,今用乙醚从黄花蒿中提取青蒿素是利用氧化还原反应原理 | |
| C. | 面粉中禁止添加CaO2、过氧化苯甲酰等增白剂,CaO2属于碱性氧化物合物,也属于离子化合物,其阴阳离子冷数比为2:l,过氧化苯甲酞属于有机物 | |
| D. | 二氧化硫有毒,产禁将其添加到任何食品和饮料中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作和现象 | 实验结论 | |
| A | 检验某溶液中是否含有SO42-时,向溶液中滴加用盐 酸酸化的BaCl2溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
| B | 检验输送氯气的管道是否发生泄漏时,用一根玻璃棒蘸取浓氨水,然后靠近管道 | 有白色烟雾产生时说明管道发生泄漏 |
| C | 检验FeCl3溶液中是否含有Fe2+时,向溶液中滴加 酸性KMnO4溶液,溶液变为无色 | 该溶液中一定含有Fe2+ |
| D | 向2mL0.1mol•L-1 硝酸银溶液中加入几滴0.1mol•L-1NaCl溶液,出现白色沉淀,再加入几滴0.1mol•L-1Na2S溶液,有黑色沉淀生成 | 该现象说明相同温度下Ksp(Ag2S)<Ksp(AgCl) |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知A、B、C、D、X、Y、Z七种短周期主族元素的原子序数依次增大,A是元素周期表中原子半径最小的,B的最高价氧化物的水化物与其氢化物反应生成盐,且B的核电荷数比Y的最外层电子数多1.C原子的最外层电子数是次外层电子数的3倍,D原子半径在同周期中除稀有气体外最大,X是同周期中简单离子半径最小的元素.请回答下列问题:
已知A、B、C、D、X、Y、Z七种短周期主族元素的原子序数依次增大,A是元素周期表中原子半径最小的,B的最高价氧化物的水化物与其氢化物反应生成盐,且B的核电荷数比Y的最外层电子数多1.C原子的最外层电子数是次外层电子数的3倍,D原子半径在同周期中除稀有气体外最大,X是同周期中简单离子半径最小的元素.请回答下列问题: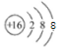 ,A与C形成的10电子分子的电子式为
,A与C形成的10电子分子的电子式为 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制氯水的氧化性强于久置氯水 | |
| B. | 过量铁与Cl2反应时生成FeCl2 | |
| C. | 1molCl2与热NaOH溶液反应生成NaClO3和NaCl时,需NaOH 2mol | |
| D. | 将饱和氯水滴到淀粉碘化钾试纸上,试纸先变蓝后变白,说明氯水具有强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 编号 | ① | ② | ③ | ④ |
| 装置 | 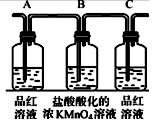 |  |  | 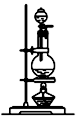 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com