
分析 ①碳酸钠和氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠;
②氯化铁和氢氧化钠溶液反应生成氢氧化铁沉淀和氯化钠;
③氯化铝和氨水反应生成氢氧化铝沉淀和氯化铵;
④碳酸钙加盐酸反应生成氯化钙、二氧化碳气体和水;
⑤碳酸氢钠和盐酸反应生成氯化钠、二氧化碳气体和水.
解答 解:①碳酸钠与氢氧化钙反应,生成碳酸钙沉淀和氢氧化钠,反应离子方程式为:Ca2++CO32-=CaCO3↓,
故答案为:Ca2++CO32-=CaCO3↓;
②氯化铁与氢氧化钠反应生成氯化钠和氢氧化铁,反应的离子方程式为:Fe3++3OH-=Fe(OH)3↓,
故答案为:Fe3++3OH-=Fe(OH)3↓;
③氯化铝和氨水:Al(OH)3不溶于过量的氨水,所以离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,
故答案为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+;
④碳酸钙加盐酸:碳酸钙与稀盐酸反应生成氯化钙、二氧化碳气体和水,反应的离子方程式为:CaCO3+2H+=Ca2++H2O+CO2↑,
故答案为:CaCO3+2H+=Ca2++H2O+CO2↑;
⑤碳酸氢钠和盐酸:向碳酸氢钠溶液中加入稀盐酸反应生成氯化钠、水和二氧化碳,该离子反应为:HCO3-+H+=C02↑+H2O,
故答案为:HCO3-+H+=C02↑+H2O.
点评 本题考查离子反应方程式的书写,题目难度中等,明确发生的化学反应是解答本题的关键,注意离子反应的书写方法即可解答,试题培养了学生灵活应用基础知识的能力及规范答题的能力.


科目:高中化学 来源: 题型:选择题
| A. | 只含一种分子的物质一定是纯净物 | |
| B. | 由Na2O2制取O2一定要加入氧化剂 | |
| C. | 金属氧化物一定是碱性氧化物 | |
| D. | 含氧酸受热分解都能生成对应的酸酐和水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 人类利用能源的三个阶段分别是:柴草时期、化石能源时期、多能源结构时期 | |
| B. | 人类使用沼气是对化学能的充分利用 | |
| C. | 海底有大量的天然气水合物-“可燃冰”,它是一种比较洁净的能源 | |
| D. | 生物质能主要指用树木、庄稼、草类等植物直接或间接提供的能量,它是不可再生的能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
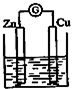 X,Y,Z,W为按原子序数由小到大排列的四种短周期的元素,X的阳离子为质子,Y原子有3个能级,各能级电子数相等,Z,W位于同一周期,Z是该周期中金属性最强的元素,W的单质是黑火药的重要成分,含有该单质的某种膏药可治疗某些皮肤病.请回答下列问题:
X,Y,Z,W为按原子序数由小到大排列的四种短周期的元素,X的阳离子为质子,Y原子有3个能级,各能级电子数相等,Z,W位于同一周期,Z是该周期中金属性最强的元素,W的单质是黑火药的重要成分,含有该单质的某种膏药可治疗某些皮肤病.请回答下列问题: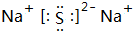 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | x>y | B. | x<y | C. | x=y | D. | 不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数为60 | B. | 原子序数为27 | C. | 中子数为27 | D. | 核外电子数为33 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com