
肼(N2H4)—空气燃料电池是一种环保型碱性燃料电池,电解质为20%~30%的KOH溶液,电池总反应为N2H4+O2=N2+2H2O。下列关于该电池工作时说法中正确的是
| A.正极的电极反应式:O2+4H++4e-=2H2O |
| B.溶液中的阴离子向正极移动 |
| C.负极的电极反应式:N2H4+4OH--4e-=4H2O+N2 |
| D.溶液的pH保持不变 |
科目:高中化学 来源: 题型:单选题
下列关于铜电极的叙述,不正确的是
| A.铜锌原电池中铜是正极 |
| B.用电解法精炼粗铜时,粗铜作阳极 |
| C.在镀件上电镀铜时可用金属铜作阳极 |
| D.电解稀硫酸制H2、O2时,铜作阳极 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
氢氧燃料电池已用于航天飞机。以30%KOH溶液为电解质溶液的这种电池在使用时的电极反应如下:2H2+ 4OH-- 4e-= 4H2O;O2+ 2H2O + 4e-= 4OH-。据此作出判断,下列说法中错误的是:
| A.H2在负极发生氧化反应 |
| B.供电时的总反应为:2H2+O2=2H2O |
| C.产物为无污染的水,属于环境友好电池 |
| D.燃料电池的能量转化率可达100% |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下图为两个原电池装置图,由此判断下列说法错误的是( )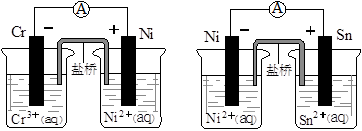
| A.当两电池转移相同电子时,生成和消耗Ni的物质的量相同 |
| B.两装置工作时,盐桥中的阴离子向负极移动,阳离子向正极移动 |
| C.由此可判断能够发生2Cr3++3Ni=3Ni2++2Cr和Ni2++Sn=Sn2++Ni的反应 |
| D.由此可判断Cr、Ni、Sn三种金属的还原性强弱顺序为:Cr>Ni>Sn |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。RFC的工作原理如图如示。下列有关说法正确的是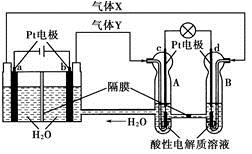
A.当有0.1 mol电子转移时,a电极产生2.24 L H2(标况)
B.b电极上发生的电极反应式为4H2O+4e-=2H2↑+4OH-
C.c电极上进行还原反应,B池中的H+可以通过隔膜进入A池
D.d电极上发生的电极反应式为O2+4H++4e-=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
按下图装置实验,若x轴表示流入阴极的电子的物质的量,则y轴可表示( )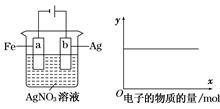
①c(Ag+) ②c(AgNO3) ③a棒的质量 ④b棒的质量
⑤溶液的pH
| A.①③ | B.③④ | C.①②④ | D.①②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
研究人员最近发明了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl。下列“水”电池在海水中放电时的有关说法正确的是
| A.正极反应式:Ag+Cl--e-=AgCl |
| B.每生成1 mol Na2Mn5O10转移2 mol电子 |
| C.Na+不断向“水”电池的负极移动 |
| D.AgCl是还原产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
目前人们掌握了可充电锌—空气电池技术,使这种电池有了更广泛的用途。这种电池使用特殊技术吸附空气中的氧,以苛性钠溶液为电解质,电池放电时的总反应为2Zn+O2=2ZnO,下列判断正确的是
| A.放电时,OH-向负极方向移动 |
| B.放电时,正极反应式为Zn+2OH--2e-=ZnO+H2O |
| C.充电时,Zn发生氧化反应 |
| D.充电时,阴极反应为O2+2H2O+4e-=4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
能用电解原理说明的问题是( )
①电解是把电能转变成化学能
②电解是化学能转变成电能
③电解质溶液导电是化学变化,金属导电是物理变化
④不能自发进行的氧化还原反应,通过电解的原理可以实现
⑤任何溶液被电解时,必然导致氧化还原反应的发生
| A.①②③④ | B.②③⑤ |
| C.③④ | D.①③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com