
| A. | 化学反应的限度决定了反应物物在该条件下的最大转化率 | |
| B. | 化学反应的限度可以通过改变条件而改变 | |
| C. | 构成原电池正极和负极的材料必须是两种金属 | |
| D. | 铜锌原电池工作时,若有13g锌被溶解,则电路中有0.4mol电子通过 |
分析 A、在不同的条件下,化学反应限度不同,当达到化学反应限度时,正逆反应速率相等但不为0,反应物的浓度和生成物的浓度不再改变,当外界条件发生改变;
B、平衡发生移动,化学反应限度变化;
C、原电池的正极可以是金属也可以是非金属石墨;
D、Zn、Cu原电池中,Zn为负极,1molZn反应转移2mol电子.
解答 解:A、当达到化学反应限度时,反应物的浓度和生成物的浓度不再改变,反应物在该条件下的转化率最大,故A正确;
B、当外界条件发生改变,平衡发生移动,化学反应限度变化,故B正确;
C、构成原电池正极和负极的材料不一定是两种金属,正极可以是惰性电极石墨,故C错误;
D、13gZn是0.2mol,负极反应13gZn,电路中通过0.4mol电子,故D正确;
故选C.
点评 本题考查化学反应平衡状态的判断、以及原电池原理,题目难度不大,注意化学反应平衡状态的本质原因是正逆反应速率相等,浓度不变是外观特征.


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源:2017届湖南省长沙市高三上学期第三次月考模拟化学试卷 题型:选择题
化学反应中的能量变化是由化学反应中旧化学健断裂时吸收的能量与化学健形成时放出的能量不同引起的。如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法中正确的是

A.1molN2(g)和1molO2(g)反应放出的能量为180kJ
B.1molN2(g)和1molO2(g)具有的总能量小于2molNO(g)具有的总能量
C.在1L的容器中发生反应.10min内N2减少了1mol,因此10min内的平均反应速率为v(NO)=0.1mol/(L·min)
D.NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 核能 | B. | 化石能源 | C. | 太阳能 | D. | 风能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. (只写一种).
(只写一种).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
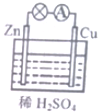
| A. | 原电池的反应本质是氧化还原反应 | B. | 电子由Cu片通过导线流向锌片 | ||
| C. | 正极反应式为Zn-2e=Zn2+ | D. | Cu为负极,Zn为正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑧ | B. | ①⑦⑧ | C. | ①③⑦⑧ | D. | ①③④⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 燃烧反应都是放热反应 | |
| B. | 对于可逆反应:aA(g)+bB(g)?bC(g)+dD(g),如果正反应放热,逆反应一定吸热 | |
| C. | 氢气燃烧生成水是一个放热的化学反应,说明1mol H2的能量高于1mol H2O的能量 | |
| D. | 石墨转化为金刚石需要吸收能量,所以石墨的化学性质更稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4 | B. | C2H4 | C. | C2H2 | D. | CH3CH2CHO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
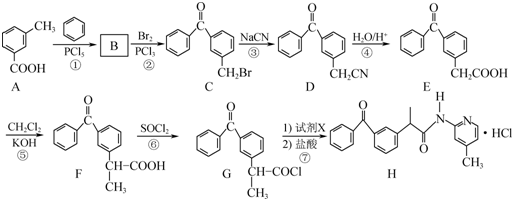
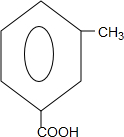 +
+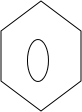 $\stackrel{PCl_{3}}{→}$
$\stackrel{PCl_{3}}{→}$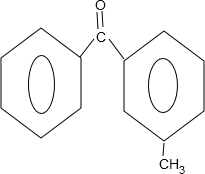 +H2O.
+H2O.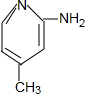 .
.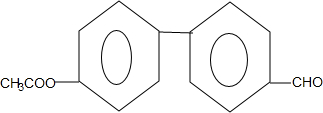 (只写一种).
(只写一种).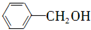 和
和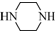 为原料制备
为原料制备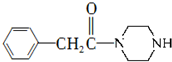 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com