
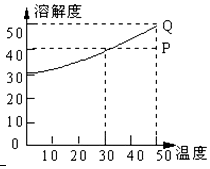
 有一种盐的溶解度曲线如图,现有组成处于P点上的该溶液,下列说法错误的是(此盐不含结晶水)( )
有一种盐的溶解度曲线如图,现有组成处于P点上的该溶液,下列说法错误的是(此盐不含结晶水)( )| A. | 50℃时,若该盐溶液含A克溶质,保持温度不变,加入A/4 g溶质,溶液必变成饱和溶液 | |
| B. | 50℃时,140g P点溶液最少需蒸发掉20g水才能形成饱和溶液 | |
| C. | 该溶液冷却至0℃时,析出溶质10 g | |
| D. | 在保持溶质及溶剂质量不变的情况下,使P点溶液达到饱和需降温20℃ |
分析 A.50℃时,100g水中最多溶解50g盐,P点100g水中溶解了40g盐;
B.饱和溶液的质量分数ω=$\frac{S}{100+S}$×100%,140g P点溶液最少需蒸发掉20g水时溶液的质量分数为$\frac{140g×\frac{40g}{100g+40g}×100%}{140g-20g}$;
C.该溶液的体积未知;
D.由图可知,30℃时溶液的溶解度为40g.
解答 解:A.由图可知,50℃时,100g水中最多溶解50g盐,而P点100g水中溶解了40g盐,再加入$\frac{40g}{4}$盐时,变成饱和溶液,故A正确;
B.50℃时,饱和溶液的质量分数ω=$\frac{S}{100+S}$×100%=$\frac{50g}{50g+100g}$×100%=33.3%,140g P点溶液最少需蒸发掉20g水时溶液的质量分数为$\frac{140g×\frac{40g}{100g+40g}×100%}{140g-20g}$=33.3%,故B正确;
C.该溶液的体积未知,所以析出溶质的质量不能计算,故C错误;
D.由图可知,30℃时溶液的溶解度为40g,所以在保持溶质及溶剂质量不变的情况下,使P点溶液达到饱和需降温50℃-30℃=20℃,故D正确;
故选C.
点评 本题考查溶液中溶质的质量分数和溶解度的计算,侧重于化学基本公式和S-T图象的综合应用,题目难度中等,注意ω=$\frac{S}{100+S}$×100%的应用.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该氨水的物质的量浓度约为6.3mol•L-1 | |
| B. | 各取5ml与等质量的水混合后,c(H2SO4)<9.2 mol•L-1,c(NH3)>6.45 mol•L-1 | |
| C. | 常温下铁不能与该硫酸反应 | |
| D. | 各取10ml于两烧杯中,再分别加入一定量的水即可得到较稀的硫酸溶液和氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向 0.1 mol/L CH3COOH 溶液中加入少量水,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$减小 | |
| B. | 将 CH3COONa 溶液从 25℃升温至 40℃,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$增大 | |
| C. | 向硝酸中加入氨水至中性,溶液中$\frac{c(N{H}_{4}^{+})}{c(N{O}_{3}^{-})}$<1 | |
| D. | 向 AgCl、AgBr 的饱和溶液中加入少量 AgNO3,溶液中$\frac{c(C{l}^{-})}{c(B{r}^{-})}$不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液氨气化时要吸收大量的热,可用作制冷剂 | |
| B. | 二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸 | |
| C. | SO2具有氧化性,可用于漂白纸浆 | |
| D. | 氯化铝是一种电解质,可用于电解法制铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1:1 | B. | 1:2 | C. | 1:3 | D. | 1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
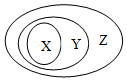 用如图表示的一些物质或概念间的从属关系中,正确的是( )
用如图表示的一些物质或概念间的从属关系中,正确的是( ) | X | Y | Z | |
| A | 非金属单质 | 非电解质 | 纯净物 |
| B | 置换反应 | 氧化还原反应 | 离子反应 |
| C | 胶体 | 分散系 | 混合物 |
| D | 酸性氧化物 | 非金属氧化物 | 氧化物 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com