
 某化学兴趣小组测定某FeCl3样品(含少量FeCl2杂质)中铁元素的质量分数,实验按以下步骤进行:①称取ag样品,置于烧杯中;②加入适量盐酸和适量蒸馏水,使样品溶解,然后准确配制成250mL溶液;③准确量取25.00mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,使反应完全;④加入过量氨水,充分搅拌,使沉淀完全;⑤过滤,洗涤沉淀;⑥将沉淀转移到坩埚内,加热、搅拌,直到固体由红褐色全部变为红棕色后,在干燥器中冷却至室温后,称量;⑦…
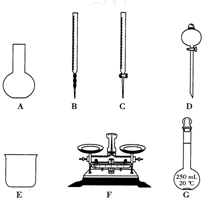
某化学兴趣小组测定某FeCl3样品(含少量FeCl2杂质)中铁元素的质量分数,实验按以下步骤进行:①称取ag样品,置于烧杯中;②加入适量盐酸和适量蒸馏水,使样品溶解,然后准确配制成250mL溶液;③准确量取25.00mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,使反应完全;④加入过量氨水,充分搅拌,使沉淀完全;⑤过滤,洗涤沉淀;⑥将沉淀转移到坩埚内,加热、搅拌,直到固体由红褐色全部变为红棕色后,在干燥器中冷却至室温后,称量;⑦…分析 (1)根据称量、溶解、配制一定物质的量浓度的溶液、准确量取溶液等操作确定所需仪器;
(2)根据氯水能将FeCl2氧化生成FeCl3;
(3)洗涤沉淀主要是为了除去沉淀表面的可溶性杂质,在过滤器中进行;
(4)氢氧化铁加热灼烧后生成氧化铁,坩埚质量是W1,坩埚与加热后固体总质量是W2,则氧化铁的质量为(W2-W1)g.氧化铁中铁元素的质量等于样品中铁元素的质量,进而计算铁元素的质量分数.
解答 解:(1)根据题中提供的仪器可知,称量时需要天平、钥匙;溶解时需要烧杯、玻璃棒;配制一定物质的量浓度的溶液时需要量筒、烧杯、玻璃棒、胶头滴管、一定规格的容量瓶;准确量取溶液需要酸式滴定管、洗耳球等,
故答案为:C、F、G;
(2)氯水能将FeCl2氧化生成FeCl3,离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,
故答案为:2Fe2++Cl2=2Fe3++2Cl-;
(3)洗涤沉淀的方法是沿玻璃棒向漏斗中沉淀上注入蒸馏水至浸没沉淀,静置让水自然流下,重复操作2~3次,
故答案为:沿玻璃棒向漏斗中沉淀上注入蒸馏水至浸没沉淀,静置让水自然流下,重复操作2~3次;
(4)铁元素质量守恒,即红棕色固体中的铁就是样品中铁,Fe2O3中铁元素的质量为(W2-W1)g×$\frac{112}{160}$,样品中铁元素的质量(W2-W1)g×$\frac{112}{160}$×$\frac{250}{25}$=7(W2-W1)g,样品中铁元素的质量分数:$\frac{7(W{\;}_{2}-W{\;}_{1})g}{ag}$×100%=$\frac{700(W{\;}_{2}-W{\;}_{1})}{a}$%,
故答案为:$\frac{700(W{\;}_{2}-W{\;}_{1})}{a}$%.
点评 本题主要考查溶液的配制、对实验原理理解、对实验操作的评价、物质含量的测定、化学计算等,难度中等,需要学生具备扎实的基础知识与分析问题、解决问题能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,11.2L氧气含氧分子数约为3.01×1023个 | |
| B. | 两个体积相同的容器,一个盛有NO,另一个盛有N2和O2的混合气体,在同温同压下两容器内气体分子总数、原子总数和气体质量也一定相等 | |
| C. | 标况下,等质量的O2和O3中所含的氧原子数目相等 | |
| D. | 将98gH2SO4溶于500ml水,得到溶液的物质的量浓度为2.0mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H1+△H2-△H3 | B. | △H3+3△H1-△H2 | C. | 3△H1+△H2-△H3 | D. | △H3+△H1-△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸氢铵溶液和足量氢氧化钠溶液混合:HCO3-+OH-═CO32-+H2O | |
| B. | 在氯化亚铁溶液中加入稀硝酸:3Fe2++4H++O3-═3Fe3++NO↑+2H2O | |
| C. | 硝酸银溶液中加入铜粉:Cu+Ag+═Cu2++Ag | |
| D. | 常温下,浓硝酸与铁屑混合:2Fe+6H+═2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用含增塑剂的聚氯乙烯薄膜作食品包装材料 | |
| B. | 用浸泡过高锰酸钾溶液的硅藻土保鲜水果 | |
| C. | 次氯酸钠溶液可用于环境的消毒杀菌 | |
| D. | 中国古代用明矾溶液的酸性清洗铜镜表面的铜锈 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
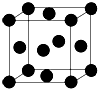 用晶体的X射线衍射法对Cu的测定得到以下结果:Cu的晶胞为面心立方最密堆积(如图),已知该晶体的密度为9.00g•cm-3,晶胞中该原子的配位数为12;Cu的原子半径为$\frac{\sqrt{2}}{4}×\root{3}{\frac{4×64}{9.00×6.06×1{0}^{23}}}$cm=1.27×10-8cm(阿伏加德罗常数为NA,列出计算表达式,不用化简).
用晶体的X射线衍射法对Cu的测定得到以下结果:Cu的晶胞为面心立方最密堆积(如图),已知该晶体的密度为9.00g•cm-3,晶胞中该原子的配位数为12;Cu的原子半径为$\frac{\sqrt{2}}{4}×\root{3}{\frac{4×64}{9.00×6.06×1{0}^{23}}}$cm=1.27×10-8cm(阿伏加德罗常数为NA,列出计算表达式,不用化简).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16g臭氧所含的原子数为NA | |
| B. | 22.4LCO气体的物质的量为1mol | |
| C. | CO的摩尔质量为28g | |
| D. | 标准状况下1mol水的体积约为22.4L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com