
| A. | 钡与水反应不如钠与水反应剧烈 | B. | 钡可以从KCl溶液中置换出钾 | ||
| C. | Ba(OH)2可与NH4Cl反应,反应放热 | D. | 碱性:KOH>Ba(OH)2>NaOH |
分析 A.元素的金属性越强,其单质的还原性越强,其单质与水或酸反应越剧烈;
B.钡的活动性介于Na和K元素之间,所以钡加入盐溶液中先和水反应;
C.Ba(OH)2可与NH4Cl反应,反应吸热;
D.元素的金属性越强,其最高价氧化物的水化物碱性越强.
解答 解:A.元素的金属性越强,其单质的还原性越强,其单质与水或酸反应越剧烈,Ba的金属性介于Na和K元素之间,所以钡与水反应比Na与水反应剧烈,故A错误;
B.钡的活动性介于Na和K元素之间,所以钡加入盐溶液中先和水反应,所以将Ba加入氯化钾溶液中先和水反应生成氢氧化钡,故B错误;
C.Ba(OH)2可与NH4Cl反应,反应吸热,故C错误;
D.元素的金属性越强,其最高价氧化物的水化物碱性越强,Ba的金属性介于Na和K元素之间,所以碱性KOH>Ba(OH)2>NaOH,故D正确;
故选D.
点评 本题考查金属元素的性质,明确金属的金属性强弱与其单质的还原性强弱、其最高价氧化物的水化物碱性强弱之间的关系是解本题关键,易错选项是C.


科目:高中化学 来源: 题型:选择题
| A. | 工业生产中常用静电除尘装置除去废气中的固体悬浮物 | |
| B. | 三氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀 | |
| C. | 一束平行光线照射豆浆时,可看到光亮的通路 | |
| D. | 万里长江流入大海处,形成长江三角洲 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 金属离子 | Fe2+ | Fe3+ | Al3- | Mg2+ | Ni2+ |
| 开始沉淀的pH值 | 6.5 | 1.6 | 3.4 | 9.4 | 7.2 |
| 完全沉淀的pH值 | 9.7 | 3.2 | 5.4 | 12.4 | 9.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤的气化和液化是使煤变成清洁能源的有效途径 | |
| B. | 煤的干馏过程属于物理变化,通过干馏可以得到焦炉气、煤焦油、焦炭等产品 | |
| C. | 工业上大量燃烧含硫燃料是形成“酸雨”的主要原因 | |
| D. | 以煤为原料可获得许多合成高分子材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
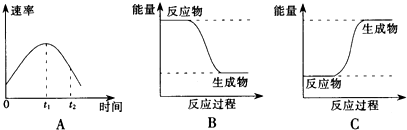
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,结构简式H2C=CH2.
,结构简式H2C=CH2.
 ,反应类型是加聚反应.
,反应类型是加聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作 | 现象 | 结论 | |
| A | 将石蜡油加强热(裂解)所产生的气体通入酸性高锰酸钾溶液中 | 溶液褪色 | 产物不都是烷烃 |
| B | 向盛有3mL鸡蛋清溶液的试管里,滴入几滴浓硝酸 | 鸡蛋清变黄色 | 蛋白质可以发生颜色反应 |
| C | 将碘酒滴到新切开的土豆片上 | 土豆片变蓝 | 淀粉遇碘元素变蓝 |
| D | 将新制Cu(OH)2与葡萄糖溶液混合加热 | 产生红色沉淀 | 葡萄糖具有还原性 |
| A. | A | B. | B | C. | C | D. | D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHB的电离方程式为:NaHB?Na-+H-+B2- | |
| B. | NaHB溶液一定呈酸性 | |
| C. | NaHB和NaOH溶液反应的离子方程式为H++OH-═H20 | |
| D. | NaHB溶液中一定存在:c(Na+)+c(H+)═c(HB-)+2c(B2-)+c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com