
【题目】CO、CO2是化石燃料燃烧后的主要产物。
(1)将体积比为2:1的CO2和CO混合气体通入有足量Na2O2固体的密闭容器中,同时不断地用电火花点燃。将残留固体溶于水,所得溶液中2c(CO32-)+c(HCO3-)____________c(Na+)(填“>”“<”或“=”) 。
(2)已知:2CO(g)+O2(g)=2CO2(g) △H=-566.0 kJ/mol;键能E(o=o)=499.0 kJ/mol
①CO(g)+O2(g)![]() CO2(g)+O(g) 的△H=____________kJ/mol
CO2(g)+O(g) 的△H=____________kJ/mol
②已知2500K时,①中反应的平衡常数为0.40。某时刻该反应体系中各物质浓度满足: c(CO)·c(O2)=c(CO2)·c(O),则此时反应____________(填向左”或“向右”)进行。
(3)已知:反应CO2(g)![]() CO(g)+O(g)在密闭容器中CO2分解实验的结果如下图1;反应2CO2(g)
CO(g)+O(g)在密闭容器中CO2分解实验的结果如下图1;反应2CO2(g)![]() 2CO(g)+O2(g)中1molCO2在不同温度下的平衡分解量如下图2,
2CO(g)+O2(g)中1molCO2在不同温度下的平衡分解量如下图2, 
①分析图1,求2min内v(CO2)=_______。
②分析图2,1500℃时反应达平衡,此时容器体积为1 L,则反应的平衡常数K=______(计算结果保留1位小数)。
(4)为探究不同催化剂对CO和H2合成CH3OH的选择性效果,某实验室控制CO和H2的初始投料比为1:3进行实验,得到如下数据:
选项 | T/K | 时间/min | 催化剂种类 | 甲醇的含量(%) |
A | 450 | 10 | CuO-ZnO | 78 |
B | 450 | 10 | CuO-ZnO-ZrO2 | 88 |
C | 450 | 10 | ZnO-ZrO2 | 46 |

①由表1可知,该反应的最佳催化剂为____________(填编号);图3中a、b、c、d四点是该温度下CO的平衡转化率的是____________。
②有利于提高CO转化为CH3OH的平衡转化率的措施有____________。
A. 使用催化剂CuO-ZnO-ZrO2 B. 适当降低反应温度
C. 增大CO和H2的初始投料比 D. 恒容下,再充入a mol CO和3a mol H2
【答案】< -33.5 向左 3×10-7 mol/(Lmin) 3.2×10-8 mol/L B cd BD
【解析】
(1)碳酸钠在溶液中水解显碱性,结合溶液中电荷守恒分析;
(2)①根据盖斯定律,将已知的热化学方程式叠加,可得待求反应的热化学方程式;
②根据Qc与K的相对大小判断;
(3)①2min内O的浓度增大0.6×10-6 mol/L,则二氧化碳减小0.6×10-6mol/L,根据v(CO2)=![]() 计算;
计算;
②根据物质反应转化关系,计算平衡时各种物质的物质的量,利用体积比等于物质的量的比,结合K的含义计算;
(4)①表中数据可知,相同条件下甲醇的含量最高时催化剂效果最好,图2中a、b、c、d四点是该温度下CO平衡转化率的必须是平衡状态下的转化率;
②由CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H1=-53.7 kJ/mol可知提高CO2转化为CH3OH平衡转化率,应使平衡向正向移动,可降低温度,增大浓度。
CH3OH(g)+H2O(g) △H1=-53.7 kJ/mol可知提高CO2转化为CH3OH平衡转化率,应使平衡向正向移动,可降低温度,增大浓度。
(1) Na2O2与CO2反应:2CO2+2Na2O2=2Na2CO3+O2,电火花不断引燃,发生反应:2CO+O2![]() 2CO2,整个过程相当于CO+Na2O2=Na2CO3,由于加入足量的Na2O2固体,则反应后的气体只能为O2,所以反应后生成物的化学式是Na2CO3、O2;Na2CO3在溶液中水解显碱性,则c(OH-)>c(H+)。溶液中电荷守恒为:2c(CO32-)+c(HCO3-)+c(OH-)=c(H+)+c(Na+),由于c(OH-)>c(H+),所以2c(CO32-)+c(HCO3-)<c(Na+);
2CO2,整个过程相当于CO+Na2O2=Na2CO3,由于加入足量的Na2O2固体,则反应后的气体只能为O2,所以反应后生成物的化学式是Na2CO3、O2;Na2CO3在溶液中水解显碱性,则c(OH-)>c(H+)。溶液中电荷守恒为:2c(CO32-)+c(HCO3-)+c(OH-)=c(H+)+c(Na+),由于c(OH-)>c(H+),所以2c(CO32-)+c(HCO3-)<c(Na+);
(2)①已知:(i)2CO(g)+O2(g)=2CO2(g) △H=-566.0 kJ/mol;
(ii)O2(g)=2O(g) △H=+499 kJ/mol;
根据盖斯定律:[(i)+ (ii)]÷2,整理可得:两个方程相加除以2即可得到CO(g)+O2(g)![]() CO2(g)+O(g) 的△H=-33.5 kJ/mol;
CO2(g)+O(g) 的△H=-33.5 kJ/mol;
②某时刻该反应体系中各物质浓度满足:c(CO)·c(O2)=c(CO2)·c(O),则Qc=![]() =1>K=0.40,则反应向左进行;
=1>K=0.40,则反应向左进行;
(3)①2min内O的浓度增大0.6×10-6 mol/L,则CO2的浓度减小0.6×10-6 mol/L,则v(CO2)=![]() =3×10-7 mol/(L·min);
=3×10-7 mol/(L·min);
②在反应开始时n(CO2)=1 mol,设生成的O2为x mol,则平衡时n(O2)=x mol,n(CO)=2x mol,n(CO2)=(1-2x) mol,由于平衡时,氧气的体积分数为0.2,则![]() =0.2,解得x=0.002,此时容器体积为1 L,则c(CO2) =0.996 mol/L,c(CO)=0.004 mol/L,c(O2)=0.002 mol/L,所以该反应的化学平衡常数K=
=0.2,解得x=0.002,此时容器体积为1 L,则c(CO2) =0.996 mol/L,c(CO)=0.004 mol/L,c(O2)=0.002 mol/L,所以该反应的化学平衡常数K=![]() mol/L≈3.2×10-8 mol/L;
mol/L≈3.2×10-8 mol/L;
(4)①表中数据可知,相同条件下甲醇的含量最高时催化剂效果最好,所以甲醇含量88%最高,催化剂CuO-ZnO-ZrO2最佳,故合理选项是B
图3中a、b、c、d四点是该温度下CO平衡转化率的必须是平衡状态下的转化率,a、b点反应未达到平衡状态,不是平衡转化率,而c、d点是平衡转化率,故合理选项是cd;
②A.使用催化剂CuO-ZnO-ZrO2 加快反应速率,但不能使化学平衡发生移动,因此不能提高CO的平衡转化率,A错误;
B.该反应的正反应是放热反应,适当降低反应温度,可以使化学平衡正向移动,可增大反应物CO的转化率,B正确;
C.增大CO和H2的初始投料比,可增大H2的转化率,CO的转化率减小,C错误;
D.恒容下,再充入a molCO和3a mol H2,相当于增大压强,中的压强,化学平衡向气体体积减小的正反应方向移动,CO转化率增大,D正确;
故合理选项是BD。


科目:高中化学 来源: 题型:
【题目】实验室用8.7g的MnO2与50mL足量的浓盐酸制取氯气
(1)求生成氯气的体积_________(标准状况)
(2)若向反应后的剩余溶液中,加入足量AgNO3溶液,生成白色沉淀57.4g,求原浓盐酸的物质的量浓度_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,它们的原子最外层电子数总和等于Z的原子序数,由这四种元素组成的一种化合物M具有如图性质,下列推断正确的是

A.原子半径:Z>Y>X>W
B.最高价氧化物对应的水化物酸性:Y>X
C.W、Y、Z组成的化合物只含共价键
D.W分别与X、Y、Z组成的二元化合物都易溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】稀氨水中存在着下列平衡:NH3·H2O![]() NH4++OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入的物质或采取的措施是
NH4++OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入的物质或采取的措施是
①NH4Cl固体;②硫酸;③NaOH固体;④水;⑤加热;⑥加入少量MgSO4固体。
A. ①②③⑤ B. ③⑥ C. ③ D. ③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知0.1 mol·L-1的醋酸溶液中存在电离平衡:CH3COOH ![]() CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是( )
CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是( )
①加少量烧碱溶液 ②升高温度 ③加少量冰醋酸 ④加水
A. ①② B. ②④ C. ③④ D. ①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(ClNO)是有机物合成中的重要试剂,其沸点为 -5.5℃,易水解。已知:AgNO2 微溶于水,能溶于硝酸,AgNO2+HNO3=AgNO3 +HNO2,某学习小组在实验室用Cl2和NO制备ClNO并测定其纯度,相关实验装置如图所示。

(1)制备 Cl2 的发生装置可以选用 _________ (填字母代号)装置,发生反应的离子方程式为________________________________________ 。
(2)欲收集一瓶干燥的氯气,选择合适的装置,其连接顺序为 a→_______→______→ _____→________→_______→______→______→______。(按气流方向,用小写字母表示,根据需要填,可以不填满,也可补充)。
(3)实验室可用下图示装置制备亚硝酰氯。其反应原理为:Cl2+2NO=2ClNO

①实验室也可用 B 装置制备 NO , X 装置的优点为___________________ 。
②检验装置气密性并装入药品,打开 K2,然后再打开 K3,通入一段时间气体,其目的是 ___________________,然后进行其他操作,当 Z 中有一定量液体生成时,停止实验。
(4)已知:ClNO 与 H2O 反应生成 HNO2 和 HCl。
①设计实验证明 HNO2 是弱酸:_________________________________________。(仅提供的试剂:1 molL-1 盐酸、 1 molL-1HNO2 溶液、 NaNO2 溶液、红色石蕊试纸、蓝色石蕊试纸)。
②通过以下实验测定ClNO 样品的纯度。取 Z 中所得液体m g 溶于水,配制成 250 mL 溶液;取出 25.00 mL 样品溶于锥形瓶中,以 K2CrO4 溶液为指示剂,用 c molL-1 AgNO3标准溶液滴定至终点,消耗标准溶液的体积为 20.00mL。滴定终点的现象是_____亚硝酰氯(ClNO)的质量分数为 _________。(已知: Ag2CrO4 为砖红色固体;Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=1×10-12)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 表示阿伏加德罗常数的值,下列说法正确的是( )
表示阿伏加德罗常数的值,下列说法正确的是( )
A.常温下![]() 的
的![]() 溶液中
溶液中![]() 与
与![]() 数目均为
数目均为![]()
B.![]() 葡萄糖和果糖的混合物中含羟基数目为
葡萄糖和果糖的混合物中含羟基数目为![]()
C.![]() 与足量
与足量![]() 反应,生成
反应,生成![]() 和
和![]() 的混合物,Na失去
的混合物,Na失去![]() 个电子
个电子
D.室温下,![]() 的
的![]() 溶液中,由水电离的
溶液中,由水电离的![]() 数目为
数目为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:
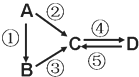
(1)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。写出②反应的离子方程式_________;④反应离子方程式__________。
(2)若A是应用最广泛的金属。④反应用到A,②⑤反应均用到同一种黄绿色气体单质。写出A与水高温下反应的化学方程式_______________________。④反应的离子方程式______________。D中加入氢氧化钠的现象__________。
(3)若A是太阳能电池用的光伏材料,B常用用于制作高档光学器材,C、D为钠盐,C的水溶液俗称泡花碱,D的溶液显碱性。④反应也是通入一种引起温室效应的主要气体。写出③反应的化学方程式________________________。⑤反应用到B,反应条件为高温,则⑤的化学方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有25 mL 2 mol·L-1Na2CO3和75 mL 1 mol·L-1的稀盐酸:①将Na2CO3溶液缓缓滴到稀盐酸中 ②将稀盐酸缓缓滴到Na2CO3溶液中,在标准状况下产生气体的体积情况( )
A.均为0.84 L
B.均为0.56 L
C.①>②
D.②>①
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com