
【题目】按要求完成下列问题
I.下列几种微粒或物质
①14C ②16O ③14N ④18O ⑤O2 ⑥O3
⑦CH3-CH3 ⑧C2H6 ⑨CH3- CH2-OH ⑩ CH3-O-CH3
(1)互为同位素的是______,(填序号,下同)质子数不同中子数相同的是______________
(2)互为同素异形体的是_________, 互为同分异构体的是_____________________
II.在25 C、101 kPa的条件下,

对于反应H2(g)+Cl2(g)= 2HCl(g), 测得生成2 mol HCI(g)时,反应过程中放出183 kJ的热量,则断开1 mol H- Cl键所需的能量是____ kJ.

III.如图所示的原电池装置中,正极的电极反应方程式是________________________
【答案】②④ ① ② ⑤ ⑥ ⑨ ⑩ 431 2H++2e-==H2 ↑
【解析】
I.具有相同质子数、不同中子数的原子为同位素;同种元素的不同单质,互为同素异形体;具有相同分子式、不同结构的有机物互为同分异构体;
II.根据焓变=反应物总键能-生成物总键能;
III.原电池装置中,正极氧化剂得电子发生还原反应。
I.(1)②16O④18O质子数均为8,中子数分别为8、10,故互为同位素的是②④,①14C②16O质子数不同分别为6、8,中子数相同均为8,质子数不同中子数相同的是① ②,故答案为:②④;① ②;
(2)⑤O2 ⑥O3是氧元素形成的两种单质,互为同素异形体的是⑤⑥,⑨CH3- CH2-OH ⑩ CH3-O-CH3 的分子式均为:C2H6O,前者是醇类,后者是醚类,互为同分异构体的是⑨ ⑩,故答案为:⑤⑥;⑨ ⑩;
II.根据焓变=反应物总键能-生成物总键能,断裂1molH-H键与1molCl-Cl键吸收的能量之和,即436kJ+243kJ=679kJ,设断开1molH-Cl键吸收的总能量为E(H-Cl),则有(436kJ+243kJ)-2×E(H-Cl)=-183kJ,则E(H-Cl)=431kJ,,故答案为:431;
III.原电池装置中,正极氧化剂得电子发生还原反应,氢离子得电子生成氢气,正极的电极反应方程式是2H++2e-==H2 ↑,故答案为:2H++2e-==H2 ↑。


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
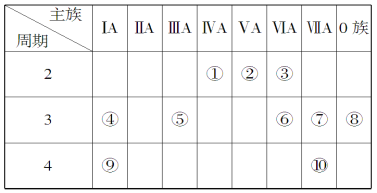
(1)元素⑦的名称为______,在周期表中的位置______________。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是_______,碱性最强的化合物的电子式是__________。
(3)用电子式表示元素④和⑥的化合物的形成过程:____________,该化合物属于______(填“共价”或“离子”)化合物。
(4)写出一种由上述元素组成的既有离子键又有共价键的物质的化学式______。
(5)⑥、⑦、⑨三种元素形成的离子,离子半径由大到小的顺序是_________(用离子符号表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用氟化钙固体和浓硫酸混合加热制HF:CaF2+H2SO4(浓)![]() CaSO4+2HF↑。下列关于该反应的说法错误的是
CaSO4+2HF↑。下列关于该反应的说法错误的是
A.该反应利用了浓硫酸的酸性和难挥发性
B.CaF2晶体中Ca2+和F-的配位数之比为1:2
C.影响H2SO4和CaSO4熔点的作用力不同
D.HF是极性分子且分子极性强于HC1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化硅(Si3N4)是一种重要的结构陶瓷材料,实验室通常利用干燥的氮气与晶体硅的粉末在1300~1400℃下反应制备氮化硅,所用装置如图所示(部分仪器已省略),下列说法错误的是

A.装置Ⅲ处省略了加热仪器酒精灯
B.装置Ⅱ所装试剂为浓硫酸
C.实验中要先对装置Ⅲ加热再打开分液漏斗活塞
D.若将晶体硅粉末分散在石棉绒中反应会更充分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】连二亚硫酸钠(Na2S2O4)俗称保险粉,常用于纺织工业、食品漂白等领域。某种Na2S2O4的生产工艺流程如图所示:若在实验室模拟该工艺流程,下列说法错误的是
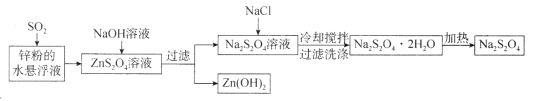
A.将锌粉投入水中形成悬浮液主要是为了加快反应速率
B.向Na2S2O4溶液中加NaCl溶液或固体对Na2S2O4的产率无明显影响
C.洗涤Na2S2O4·2H2O时用冰水效果好于常温蒸馏水
D.该流程中涉及化合反应、分解反应、复分解反应,不涉及氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知酸性:![]() > H2CO3>
> H2CO3>![]() >HCO3-,综合考虑反应物的转化率和原料成本等因素,将
>HCO3-,综合考虑反应物的转化率和原料成本等因素,将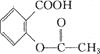 转变为
转变为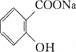 的最佳方法是
的最佳方法是
A. 与稀H2SO4共热后,加入足量的NaOH溶液
B. 与稀H2SO4共热后,加入足量的NaHCO3溶液
C. 与足量的NaOH溶液共热后,再通入足量CO2
D. 与足量的NaOH溶液共热后,再加入适量H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下列实验装置进行的相应实验,不能达到实验目的的是
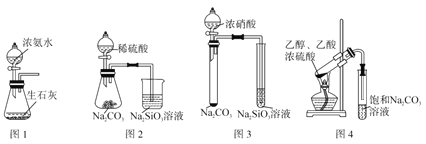
A.用图1所示装置制取氨气
B.用图2所示装置证明非金属性强弱:S>C> Si
C.用图3所示装置证明酸性强弱:硝酸>碳酸>硅酸
D.用图4所示装置制备少量的乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的性质与应用均正确且二者具有对应关系的是 ( )
A.钠钾合金的导热性强,可用作快中子反应堆的热交换剂
B.氧化铁能与酸反应,可用于制作红色涂料
C.![]() 溶液显碱性,可用于除去锅垢中的硫酸钙
溶液显碱性,可用于除去锅垢中的硫酸钙
D.常温下铝与浓硝酸不反应,常用铝罐车运输浓硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蛋氨酸铜[Cux(Met)y,Met表示蛋氨酸根离子]是一种新型饲料添加剂。为确定蛋氨酸铜[Cux(Met)y]的组成,进行如下实验:
(1)称取一定质量的样品于锥形瓶中,加入适量的蒸馏水和稀盐酸,加热至全部溶解,冷却后将溶液分成两等份。
②取其中一份溶液,调节溶液pH在6~8之间。加入0.1000 mol/LI2的标准溶液25.00 mL,充分反应后滴入2~3滴指示剂X,用0.1000 mol/LNa2S2O3标准溶液滴定至蓝色恰好褪去,发生反应:![]() 。消耗Na2S2O3标准溶液22.00 mL(蛋氨酸与I2反应时物质的量之比为1:1,产物不与Na2S2O3发生反应)。
。消耗Na2S2O3标准溶液22.00 mL(蛋氨酸与I2反应时物质的量之比为1:1,产物不与Na2S2O3发生反应)。
③向另一份溶液中加入NH3·H2O-NH4Cl缓冲溶液,加热至70℃左右,滴入2-3滴指示剂PAN,用0.02500 mol/LEDTA (Na2H2Y)标准溶液滴定其中Cu2+(离子方程式为Cu2++H2Y2--=CuY2-+2H+),消耗EDTA标准溶液28.00 mL。
(1)指示剂X为 ____。
(2)用Na2S2O3标准液滴定时,若pH过小,会有S和SO2生成。写出S2O32-与H+反应的离子方程式 ___________ 。
(3)若滴定管水洗后未用EDTA标准溶液润洗,测得Cu2+的物质的量将____(填“偏大”、“偏小”或“不变”)。
(4)通过计算确定蛋氨酸铜[Cux(Met)y]的化学式(写出计算过程)________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com