
【题目】(1)基态溴原子的价层电子轨道排布式为________。第四周期中,与溴原子未成对电子数相同的金属元素有_______种。
(2)铍与铝的元素性质相似。下列有关铍和铝的叙述正确的有___________(填标号)。
A.都属于p区主族元素B.电负性都比镁大
C.第一电离能都比镁大D.氯化物的水溶液pH均小于7
(3)Al元素可形成[AlF6]3-、[AlCl4]-配离子,而B元素只能形成[BF4]-配离子,由此可知决定配合物中配位数多少的因素是________________;[AlCl4]-的立体构型名称为______。
(4)P元素有白磷、红磷、黑磷三种常见的单质。
①白磷(P4)易溶于CS2,难溶于水,原因是________________
②黑磷是一种黑色有金属光泽的晶体,是一种比石墨烯更优秀的新型材料。白磷、红磷都是分子晶体,黑磷晶体与石墨类似的层状结构,如图所示。下列有关黑磷晶体的说法正确的是_________。

A.黑磷晶体中磷原子杂化方式为sp2杂化
B.黑磷晶体中层与层之间的作用力是分子间作用力
C.黑磷晶体的每一层中磷原子都在同一平面上
D.P元素三种常见的单质中,黑磷的熔沸点最高
(5)F2中F-F键的键能(157kJ/mol)小于Cl2中Cl-Cl键的键能(242.7kJ/mol),原因是_________。
(6)金属钾的晶胞结构如图。若该晶胞的密度为a g/cm3,阿伏加得罗常数为NA,则表示K原子半径的计算式为______。

【答案】![]() 4 BD 中心原子半径、配位原子的半径 正四面体 P4 、CS2是非极性分子,H2O是极性分子,根据相似相溶原理,P4难溶于水 BD F的原子半径小,孤电子对之间的斥力大
4 BD 中心原子半径、配位原子的半径 正四面体 P4 、CS2是非极性分子,H2O是极性分子,根据相似相溶原理,P4难溶于水 BD F的原子半径小,孤电子对之间的斥力大 ![]()
【解析】
(1)溴原子为35号元素,基态原子价层电子排布式[Ar] 3d104s24p5,电子排布图为:![]() ;,溴原子未成对电子数为1,与溴原子未成对电子数相同的金属元素有:K、Sc、Cr、Cu,共4种;
;,溴原子未成对电子数为1,与溴原子未成对电子数相同的金属元素有:K、Sc、Cr、Cu,共4种;
(2)铍与相邻主族的铝元素性质相似。A.Be属于s区,Al属于P区,故A错误;B.电负性都比镁大,故B正确;C.元素Be的第一电离能比Mg大,元素Al的第一电离能比Mg小,故C错误;D.氯化物的水溶液均发生水解,溶液显酸性,则PH<7, D项正确。答案选BD;
(3)B3+离子半径明显小于Al3+,则Al元素可形成[AlF6]3-,[AlCl4]-配离子,而B只能形成[BF6]3-配离子,因此,决定配合物中配位数多少的因素是中心原子(或例子)及配位原子半径的大小;[AlCl4]-的配位数是4,故立体构型为正四面体形;
(4)①P4, CS2是非极性分子,H2O是极性分子,根据相似相溶原理,P4难溶于水;②A. 由结构可知G中磷原子杂化方式为sp3杂化,故A错误;B. G中层与层之间的作用力是分子间作用力,故B正确;C. 石墨中碳原子为sp2杂化,每层原子均在同一平面内,但磷原子杂化方式为sp3杂化,每一层的各原子不可能在同一平面内,故C错误;D. 黑磷为原子晶体,而其它二种单质为分子晶体,则黑磷的熔沸点最高,故D正确;所以答案为BD;
(5)可以根据键长的大小来判断,具体来说就是根据相结合的2个原子的半径来比较,半径越小键能越大,而F的原子半径小,孤电子对之间的斥力大,导致F2中F-F键的键能(157kJ/mol)小于Cl2中Cl-Cl键的键能(242.7kJ/mol);
(6)金属钾的晶胞结构为体心立方,晶胞中K原子数目为:1+8×![]() =2,阿伏加德罗常数为NA,K原子的摩尔质量为M,故晶胞质量为:
=2,阿伏加德罗常数为NA,K原子的摩尔质量为M,故晶胞质量为:![]() ;设K原子半径为r,设晶胞棱长为l,晶胞中体对角线为4r,则(4r)2=l2+l2+l2,则l=
;设K原子半径为r,设晶胞棱长为l,晶胞中体对角线为4r,则(4r)2=l2+l2+l2,则l=![]() r,晶胞体积V=l3=(
r,晶胞体积V=l3=(![]() r)3,若该晶胞的密度为ag/cm3,则(
r)3,若该晶胞的密度为ag/cm3,则(![]() r)3×a=
r)3×a=![]() ,且M=39 g/mol整理得:r=
,且M=39 g/mol整理得:r=![]() 。
。


科目:高中化学 来源: 题型:
【题目】键线结构式是以线表示共价键,每个折点和线端点处表示一个碳原子,并省略书写氢原子的一种表示有机化合物结构的方式,如异丁烷(![]() )要表示为“
)要表示为“![]() ”,请分析这一表示方式的要领,试用键线结构式写出戊烷(C5H12)的同分异体____、___、___。
”,请分析这一表示方式的要领,试用键线结构式写出戊烷(C5H12)的同分异体____、___、___。
通过解题你是如何筛选并运用信息的 ______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁—锑液态金属储能电池工作原理如下图所示,该电池所用液体密度不同,在重力作用下分为三层,工作时中间层熔融盐的组成及浓度不变。下列说法不正确的是
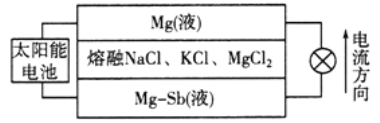
A. 放电时,Mg(液)层的质量减小
B. 放电时,正极反应为:Mg2++2e===Mg
C. 该电池充电时,Mg—Sb(液)层的质量增大
D. 该电池充电时,C1向下层方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲、乙两种物质:

(1)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):
![]()
其中反应I的反应类型是___________,反应II的条件是_______________,反应III的化学方程式为___________________________________(不需注明反应条件)。
(2)下列物质不能与乙反应的是 (选填序号)。
a.金属钠 b.溴水 c.碳酸钠溶液 d.乙酸
(3)乙有多种同分异构体,任写其中一种能同时满足下列条件的同分异构体结构简式 。
a.苯环上的一氯代物有两种
b.遇FeCl3溶液显示紫色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列转化的化学方程式,注明反应类型。
(1)甲苯→TNT ___________________
(2)苯乙烯→聚苯乙烯__________________
(3)1,3—丁二烯与溴1,4—加成__________________
(4)2-甲基-2-溴丙烷和氢氧化钾乙醇溶液共热___________________
(5)苯甲醇在铜催化下和氧气反应__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCl2是一种用途广泛的化工产品。由于在水溶液中难以得到高纯度的FeCl2,某课题小组设计氯化铁和氯苯反应制得高纯度的FeCl2。
(查阅资料)①在加热条件下,氯化铁遇水剧烈水解。
②2FeCl3 +C6H5Cl →C6H4Cl2 + 2FeCl2 + HCl↑
③有关数据如下:
C6H5Cl(氯苯) | C6H4Cl2(对二氯苯) | FeCl3 | FeCl2 | |
式量 | 112.5 | 147 | 162.5 | 127 |
溶解性 | 不溶于水,易溶于苯 | 溶于水,不溶于C6H5Cl、C6H4Cl2、苯 | ||
熔点/℃ | -45 | 53 | —— | —— |
沸点/℃ | 132 | 173 | —— | —— |
(实验过程)按下图装置,在三颈烧瓶中放入a g无水氯化铁和过量的氯苯,控制反应温度在128~139℃加热3h,冷却,分离提纯A中物质得到产品。
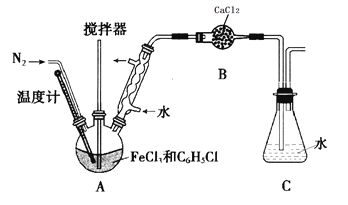
回答下列问题:
(1)实验装置中,仪器B的名称是________________。
(2)反应前后都需要通入N2的目的是_____________。
(3)实验过程中控制反应温度128~139℃,C6H5Cl不会有明显损失,原因是_____________。
(4)充分反应后,冷却。对三颈烧瓶内的物质进行过滤,用苯洗涤沉淀,干燥得到产品。回收滤液中C6H5Cl的方案为_______________。
(5)经检验产品中不含有FeCl3。取少量所得产品溶解于盐酸中,配制成溶液。向盛有H2O2溶液的试管中加入几滴配制的溶液,溶液变成棕黄色,一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成。产生气泡的原因是__________;生成沉淀的原因是(用平衡移动原理解释)__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关煤、石油、天然气等资源的说法正确的是( )
A.煤就是碳,属于单质
B.石油产品都可用于加成反应
C.天然气是一种清洁的化石燃料
D.石油裂解得到的汽油是纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A. 78gNa2O2固体中含有的离子数之和为3NA
B. 标准状况下22.4LCl2通入足量水中,反应中转移的电子数为NA
C. 18gD2O所含有的质子数、电子数均为10NA
D. pH=1的醋酸溶液中含有的H+数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学学习小组进行如下实验测定 H2C2O4·xH2O 中 x 值已知:M(H2C2O4)=90gmol-1
① 称取1.260 g 纯草酸晶体,将草酸制成 100.00 mL 水溶液为待测液;
② 取25.00 mL 待测液放入锥形瓶中,再加入适量的稀 H2SO4;
③ 用浓度为 0.05 000 mol·L-1 的 KMnO4标准溶液进行滴定。
(1)请写出滴定中发生反应的离子方程式________________________。
(2)某学生的滴定方式(夹持部分略去)如下,最合理的是_____(选填 a、b)。
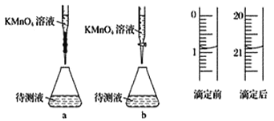
(3)由图可知消耗 KMnO4 溶液体积为________mL。
(4)滴定过程中眼睛应注视_______________,滴定终点锥形瓶内溶液的颜色变化为_______。
(5)通过上述数据,求得 x=_____。
a.若由于操作不当,滴定结束后滴定管尖嘴处有一气泡, 引起实验结果_____(填“偏大”、“偏小”或“无影响”);
b.若在接近终点时,用少量蒸馏水将锥形瓶冲洗一下,再继续滴定至终点,则所测结果_______(填“偏大”、“偏小”或“无影响”);
c.若在达到滴定终点时仰视读数,则所得结果________(填“偏大”、“偏小”或“无影响”);
d.若其它操作均正确,滴定前未用标准 KMnO4 溶液润洗滴定管,引起实验结果_________(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com