
【题目】在一定条件下,将3mol A和1mol B两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)xC(g)+2D(g).2min后该反应达到平衡,生成0.8mol D,并测得C的浓度为0.2mol/L,下列判断错误的是( )
A.x=1
B.2 min内A的反应速率为0.3 mol/(Lmin)
C.B的转化率为40%
D.若混合气体的密度不变,则表明该反应达到平衡状态
【答案】D
【解析】解:A.平衡时生成的C的物质的量为0.2molL﹣1×2L=0.4mol,物质的量之比等于化学计量数之比,故0.4mol:0.8mol=x:2,解得x=1,故A正确;B.2min内生成0.8mol D,故2 min内D的反应速率v(D)= ![]() =0.2 mol(Lmin)﹣1 , 速率之比等于化学计量数之比,故v(A)=
=0.2 mol(Lmin)﹣1 , 速率之比等于化学计量数之比,故v(A)= ![]() v(D)=
v(D)= ![]() ×0.2 mol(Lmin)﹣1=0.3 mol(Lmin)﹣1 , 故B正确;
×0.2 mol(Lmin)﹣1=0.3 mol(Lmin)﹣1 , 故B正确;
C.2min末该反应达到平衡,生成0.8mol D,由方程式3A(g)+B(g)xC(g)+2D(g)可知,参加反应的B的物质的量为:0.8mol× ![]() =0.4mol,故B的转化率为
=0.4mol,故B的转化率为 ![]() =100%=40%,故C正确;
=100%=40%,故C正确;
D.容器的容积不变,混合气体的质量不变,密度为定值,始终不变,故混合气体的密度不变,不能说明反应达到平衡状态,故D错误;
故选D.
【考点精析】本题主要考查了化学平衡的计算的相关知识点,需要掌握反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%才能正确解答此题.


科目:高中化学 来源: 题型:
【题目】高炉炼铁过程中发生反应: ![]() Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g) ![]() Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如表,下列说法正确的是( )
Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如表,下列说法正确的是( )
温度/°C | 1000 | 1150 | 1300 |
平衡常数 | 4.0 | 3.7 | 3.5 |
A.△H>0
B.1000℃时,在固定体积的密闭容器中,某时刻测得上述体系中,CO,CO2的物质的量分别为0.5mol、1.8mol,此时反应向正反应方向进行
C.其他条件不变,向平衡体系充入CO2气体,K值减小
D.其他条件不变,升高温度,可以提高CO的平衡转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(多选)等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生气体体积V的数据,根据数据绘制得到如图,则曲线a、b、c、d所对应的实验组别可能是( )
组别 | c(HCl)(mol/L) | 温度(℃) | 状态 |
1 | 2.0 | 25 | 块状 |
2 | 2.5 | 30 | 块状 |
3 | 2.5 | 50 | 块状 |
4 | 2.5 | 30 | 粉末状 |
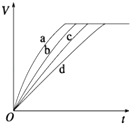
A.4﹣3﹣2﹣1
B.1﹣2﹣3﹣4
C.3﹣4﹣2﹣1
D.1﹣2﹣4﹣3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的叙述正确的是( )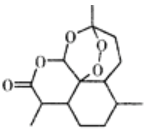
A.治疗疟疾的青蒿素(如右图),分子式为C15H20O5
B.甲苯苯环上的一个氢原子被-C3H6Cl取代,形成的同分异构体有9种
C.对三联苯 ![]() 分子中至少有16个原子共平面
分子中至少有16个原子共平面
D.油脂和乙烯在一定条件下都能与水反应,且反应类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究FeSO4和Cu(NO3)2的混合物中各组分的含量,现设计如下流程,下列叙述中不正确的是( )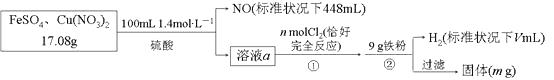
A.n=0.02
B.V=2240
C.m=3.2
D.元混合物中FeSO4的质量分数约为89%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO是合成尿素、甲酸的原料。
(1)在100 kPa和T K下,由稳定单质生成1 mol化合物的焓变称为该物质在T K时的标准摩尔生成焓,用符号ΔHm0表示。已知石墨和CO的标准燃烧热分别为393.5 kJmol1和283.0 kJmol1 , 则CO(g)的ΔHm0=。
(2)合成尿素的反应:2NH3(g) + CO(g) == CO(NH2)2(g) + H2(g) ΔH =81.0 kJmol1。
①T ℃时,在体积为2 L的恒容密闭容器中,将2 molNH3和1 mol CO混合发生反应,5 min时,NH3的转化率为80%。则0~5 min内的平均反应速率为v(CO)=。
②已知:
温度/K | 398 | 498 | … |
平衡常数(K) | 126.5 | K1 | … |
则:K1126.5(填“>”或“<”);其判断理由是。
③若保持恒温恒容条件,将物质的量之和为3 mol的NH3和CO以不同的氨碳比进行反应,结果如图所示: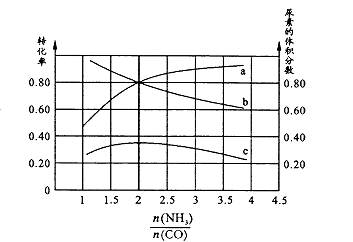
若图中c表示平衡体系中尿素的体积分数,则a表示的转化率。
当 ![]() =时,尿素含量最大;此时,对于该反应既能增大正反应速率又能使平衡正向移动的措施是(写一种)。
=时,尿素含量最大;此时,对于该反应既能增大正反应速率又能使平衡正向移动的措施是(写一种)。
(3)通过人工光合作用可将CO转化成HCOOH。
①已知常温下,浓度均为0.1 molL1的HCOOH和HCOONa混合溶液pH =3.7,则HCOOH的电离常数Ka的值为(已知lg2=0.3)。
②用电化学可消除HCOOH对水质造成的污染,其原理是电解CoSO4、稀硫酸和HCOOH混合溶液,用电解产生的Co3+将HCOOH氧化成CO2。
Co3+氧化HCOOH的离子方程式为;
忽略体积变化,电解前后Co2+的浓度将(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去NaNO3中少量NaCl、Ca(NO3)2杂质,所用试剂及顺序正确的是( )
A. Na2CO3、AgNO3、HNO3B. AgNO3、Na2CO3、HCl
C. AgNO3、Na2CO3、HNO3D. AgNO3、K2CO3、HNO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com