
 A�ӽ��� ϵ�д�
A�ӽ��� ϵ�д� ȫ�Ų��Ծ�ϵ�д�
ȫ�Ų��Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 ��2011?����һģ���Ȼ��У�C6H5CH2Cl����һ����Ҫ���л�����ԭ�ϣ��㷺Ӧ����ҽҩ��Ⱦ�ϡ������ϵ��л�������Ʒ���Ʊ����Ȼ���Ϊ��ɫҺ�壬����ǿ�ҵĴ������ã��е�Ϊ179.4�棬������ˮ���ɻ������Ҵ����ȷµȶ����л��ܼ�����ҵ�ϲ��üױ�����������ڹ��������·�Ӧ�ϳ��Ȼ��У�Ϊ̽����ͬ��ǿ�����Ժϳɲ��ʵ�Ӱ�죬��Ҫ�Բ�ͬ��ǿ�����µĴֲ�Ʒ���д��ȼ�⣮ÿһ���ⰴ�����²�����У�
��2011?����һģ���Ȼ��У�C6H5CH2Cl����һ����Ҫ���л�����ԭ�ϣ��㷺Ӧ����ҽҩ��Ⱦ�ϡ������ϵ��л�������Ʒ���Ʊ����Ȼ���Ϊ��ɫҺ�壬����ǿ�ҵĴ������ã��е�Ϊ179.4�棬������ˮ���ɻ������Ҵ����ȷµȶ����л��ܼ�����ҵ�ϲ��üױ�����������ڹ��������·�Ӧ�ϳ��Ȼ��У�Ϊ̽����ͬ��ǿ�����Ժϳɲ��ʵ�Ӱ�죬��Ҫ�Բ�ͬ��ǿ�����µĴֲ�Ʒ���д��ȼ�⣮ÿһ���ⰴ�����²�����У��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ���㽭ʡ������ѧ�߶���ѧ����ĩ���Ի�ѧ�Ծ����������� ���ͣ�ʵ����
��12�֣���1����˾ƥ����������Ӧ����㷺�Ľ��ȡ���ʹ�Ϳ���ҩ������ˮ���������ֽ⣬�ֽ��¶�Ϊ128��135�档ijѧϰС����ʵ������ˮ���ᣨ���ǻ������ᣩ�������[(CH3CO)2O]Ϊ��Ҫԭ�Ϻϳɰ�˾ƥ�֣��Ʊ������������̣��ԣ���
��д���Ʊ���˾ƥ�ֵĻ�ѧ����ʽ ��
�����ؽᾧ�ᴿ���ᴿ��˾ƥ�֡��������£�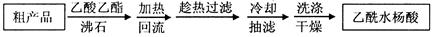
���Ȼ�����װ����ͼ��ʾ��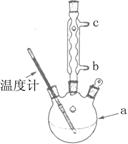
��ʹ���¶ȼƵ�Ŀ���� ��
������ˮ������������ �����b����c������
���ؽᾧ�ᴿ�����ò�Ʒ���л����ʽ��ٵ�ԭ�� ��
�����Ʒ���Ƿ���ˮ����Ļ�ѧ������ ��
��2���Ȼ��У�C6H5CH2Cl��Ҳ��һ����Ҫ���л�����ԭ�ϡ���ҵ�ϲ��üױ�����������ڹ��������·�Ӧ�ϳ��Ȼ��С�Ϊ̽����ͬ��ǿ�����Ժϳɲ��ʵ�Ӱ�죬��Ҫ�Բ�ͬ��ǿ�����µĴֲ�Ʒ(���ױ�)���д��ȼ�⡣ÿһ���ⰴ�����²�����У�
| A����ȡ0��300 g��Ʒ�� |
| B������Ʒ��25 mL 4 mol��L-lNaOH��Һ��������ƿ�л�ϣ�ˮԡ���Ȼ���lСʱ��ֹͣ���ȣ������ķ�ӦΪ��C6H5CH2Cl+NaOH��C6H5CH2OH+ NaCl���� |
| C����������ƿ�м���50 mL 2 mol��L-l HNO3����Ͼ��ȡ� |
| D����������ƿ����Һȫ��ת�Ƶ�100 mL����ƿ�У���ˮ���ݡ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013���㽭ʡ�߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
��12�֣���1����˾ƥ����������Ӧ����㷺�Ľ��ȡ���ʹ�Ϳ���ҩ������ˮ���������ֽ⣬�ֽ��¶�Ϊ128��135�档ijѧϰС����ʵ������ˮ���ᣨ���ǻ������ᣩ�������[(CH3CO)2O]Ϊ��Ҫԭ�Ϻϳɰ�˾ƥ�֣��Ʊ������������̣��ԣ���
��д���Ʊ���˾ƥ�ֵĻ�ѧ����ʽ ��
�����ؽᾧ�ᴿ���ᴿ��˾ƥ�֡��������£�
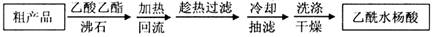
���Ȼ�����װ����ͼ��ʾ��
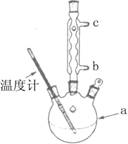
��ʹ���¶ȼƵ�Ŀ���� ��
������ˮ������������ �����b����c������
���ؽᾧ�ᴿ�����ò�Ʒ���л����ʽ��ٵ�ԭ�� ��
�����Ʒ���Ƿ���ˮ����Ļ�ѧ������ ��
��2���Ȼ��У�C6H5CH2Cl��Ҳ��һ����Ҫ���л�����ԭ�ϡ���ҵ�ϲ��üױ�����������ڹ��������·�Ӧ�ϳ��Ȼ��С�Ϊ̽����ͬ��ǿ�����Ժϳɲ��ʵ�Ӱ�죬��Ҫ�Բ�ͬ��ǿ�����µĴֲ�Ʒ(���ױ�)���д��ȼ�⡣ÿһ���ⰴ�����²�����У�
A.��ȡ0��300 g��Ʒ��
B.����Ʒ��25 mL 4 mol��L-lNaOH��Һ��������ƿ�л�ϣ�ˮԡ���Ȼ���lСʱ��ֹͣ���ȣ������ķ�ӦΪ��C6H5CH2Cl+NaOH��C6H5CH2OH+ NaCl����
C.��������ƿ�м���50 mL 2 mol��L-l HNO3����Ͼ��ȡ�
D.��������ƿ����Һȫ��ת�Ƶ�100 mL����ƿ�У���ˮ���ݡ�
E.������ƿ��ȡ��25.00 mL��Һ����ƿ�У�����6.00 mL 0.100 mol��L-1AgNO3��Һ����Ͼ��ȡ�
F.����ƿ�е��뼸��NH4Fe(SO4)2��Һ��Ϊָʾ������0.0250 mol��L-1 NH4SCN��Һ�ζ�ʣ���AgNO3��
G.�ظ�E��F�������Σ�����0.0250 mol��L1NH4SCN��Һ��ƽ��ֵΪ4.00mL��
����֪��NH4SCN+ AgNO3= AgSCN��+NH4NO3����������ʵ����Ϣ�ش�����������⣺
��C�������������Ŀ���� ��
����F��������У��жϴﵽ�ζ��յ�������� ��
�۸ò�Ʒ�Ĵ���Ϊ �����뱣��2λС����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
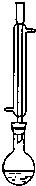 �Ȼ��У�C6H5CH2Cl����һ����Ҫ���л�����ԭ�ϣ��㷺Ӧ����ҽҩ��Ⱦ�ϡ������ϵ��л�������Ʒ���Ʊ����Ȼ���Ϊ��ɫҺ�壬����ǿ�ҵĴ������ã��е�Ϊ179.4�棬������ˮ���ɻ������Ҵ����ȷµȶ����л��ܼ�����ҵ�ϲ��üױ�����������ڹ��������·�Ӧ�ϳ��Ȼ��У�Ϊ̽����ͬ��ǿ�����Ժϳɲ��ʵ�Ӱ�죬��Ҫ�Բ�ͬ��ǿ�����µĴֲ�Ʒ���д��ȼ�⣮ÿһ���ⰴ�����²�����У�
�Ȼ��У�C6H5CH2Cl����һ����Ҫ���л�����ԭ�ϣ��㷺Ӧ����ҽҩ��Ⱦ�ϡ������ϵ��л�������Ʒ���Ʊ����Ȼ���Ϊ��ɫҺ�壬����ǿ�ҵĴ������ã��е�Ϊ179.4�棬������ˮ���ɻ������Ҵ����ȷµȶ����л��ܼ�����ҵ�ϲ��üױ�����������ڹ��������·�Ӧ�ϳ��Ȼ��У�Ϊ̽����ͬ��ǿ�����Ժϳɲ��ʵ�Ӱ�죬��Ҫ�Բ�ͬ��ǿ�����µĴֲ�Ʒ���д��ȼ�⣮ÿһ���ⰴ�����²�����У��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��10�֣��ױ�����������ڹ����·�Ӧ�����Ȼ��У������з��������ֲ�Ʒ�Ĵ��ȣ���ȡ0.255g��Ʒ����25 mL 4mol?L-1��������ˮ��Һ��100 mLԲ����ƿ�л�ϣ����Ȼ���1Сʱ���������£�����50 mL20%�������25.00mL 0.1000mol?L-1������ˮ��Һ����������0.1000mol?L-1NH4SCNˮ��Һ�ζ�ʣ��������������������Ϊָʾ����������6.75 mL��
5-1 д���������̵ķ�Ӧ����ʽ��
5-2 ������Ʒ���Ȼ��е�����������%����
5-3 ͨ���������ⶨ���������Ʒ���Ȼ��е�ʵ�ʺ�����ָ��ԭ��
5-4 �������������Ƿ��������ȱ��Ĵ��ȷ�������˵�����ɡ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com