
NM3和D 58是正处于临床试验阶段的小分子抗癌药物,结构如下:
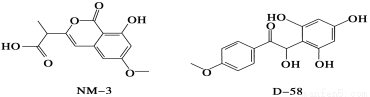
关于NM3和D58的叙述,错误的是
A.都能与NaOH溶液反应,原因不完全相同
B.都能与溴水反应,原因不完全相同
C.都不能发生消去反应,原因相同
D.遇FeCl3溶液都显色,原因相同
 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源:2017届河北省高三上学期周考(8.28)化学试卷(解析版) 题型:推断题
某强碱性溶液可能含有的离子是K+、NH4+、A13+、A1O2-、SO42-、SiO32-、CO32-、Cl-中的某几种离子,现进行如下实验:
I.取少量的溶液用硝酸酸化后,加Ba(NO3)2溶液,无沉淀生成。
II.另取少量溶液加入盐酸,其现象是:一段时间保持原样后,开始产生沉淀并逐渐增多,沉淀量基本不变后产生一种气体,最后沉淀逐渐减少至消失。
(1)原溶液中肯定存在的离子是_________,肯定不存在的离子是_________。
(2)己知一定量的原溶液中加入5mL0.2 mol/L盐酸时,沉淀会完全消失,加入足量的硝酸银溶液可得到沉淀0.187g,则原溶液中是否含有Cl-?
(3)按照反应顺序逐步书写出II中发生反应的离子反应方程式
①__________________;②______________________;
③__________________;④______________________;
⑤___________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二上入学考试化学试卷(解析版) 题型:选择题
已知 1g 氢气完全燃烧生成水蒸气时放出热量 121kJ,且氧气中1molO=O 键完全断裂时吸收热量 496kJ,水蒸气中 1molH—O 键 形成时放出热量 463kJ,则氢气中 1molH—H 键断裂时吸收热量为
A.920kJ B.557kJ C.436kJ D.188kJ
查看答案和解析>>
科目:高中化学 来源:2017届湖北省枣阳市高三上学期8月调研化学试卷(解析版) 题型:推断题
下图为周期表中的一部分。已知A、B、C、D均为短周期元素,A与D原子序数之和为C原子序数的1 .5倍。

(1)B元素符号是: _______、D在元素周期表中第_______族。
(2)四种元素中原子半径最大的是(填元素符号)_______,B、C、D三种离子中半径最大的是(填离子符号)_______。
(3)B比C的氢化物的沸点高是因为_____ __;A、D两元素的气态氢化物相互反应的生成物的电子式: ,其中存在_______键、_______(填“极性”或“非极性”)共价键。
(4)写一个离子方程式证明C和D的非金属性相对强弱: 。
查看答案和解析>>
科目:高中化学 来源:2017届湖北省枣阳市高三上学期8月调研化学试卷(解析版) 题型:选择题
如图是利用一种微生物将废水中的有机物(假设是淀粉)的化学能直接转化为电能,并利用此电能在铁上镀铜,下列说法中正确的是

A.质子透过离子交换膜由右向左移动
B.铜电极应与X相连接
C.M电极反应式:(C6H10O5)n + 7nH2O-24ne-= 6nCO2↑ + 24nH+
D.当N电极消耗0.25 mol气体时,则铁电极增重16 g
查看答案和解析>>
科目:高中化学 来源:2017届湖北省枣阳市高三上学期8月调研化学试卷(解析版) 题型:选择题
如右图所示的铜锌原电池中,铜电极为
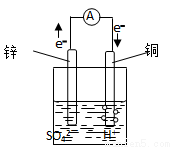
A.负极 B.正极
C.发生还原反应的一极 D.发生氧化反应的一极
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三第一次月考理综化学试卷(解析版) 题型:实验题
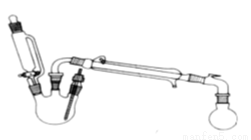
某研究性小组探究乙酸乙酯的反应机理,实验如下:
CH3COOH + C2H5OH  CH3COOC2H5 + H2O
CH3COOC2H5 + H2O
投料 1 : 1 CH3COOH转化率 65%
1 : 10 CH3COOH转化率 97%
(在120 ℃下测定)
已知:相关物理性质(常温常压)
密度g/mL | 熔点/℃ | 沸点/℃ | 水溶性 | |
乙醇 | 0.79 | -114 | 78 | 溶 |
乙酸 | 1.049 | 16.2 | 117 | 溶 |
乙酸乙酯 | 0.902 | ?84 | 76.5 | 不溶 |
合成反应:
在三颈瓶中加入乙醇5 mL,硫酸5 mL,2小片碎瓷片。漏斗加入乙酸14.3 mL ,乙醇20 mL。冷凝管中通入冷却水后,开始缓慢加热,控制滴加速度等于蒸馏速度,反应温度不超过120 ℃。
分离提纯:
将反应粗产物倒入分液漏斗中,依次用少量饱和的Na2CO3溶液、饱和NaCl溶液、饱和CaCl2溶液洗涤,分离后加入无水碳酸钾,静置一段时间后弃去碳酸钾。最终通过蒸馏得到纯净的乙酸乙酯。
回答下列问题:
(1)酯化反应的机理
用乙醇羟基氧示踪
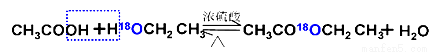
用醋酸羟基氧示踪

含氧18水占到总水量的一半,酯也一样。这个实验推翻了酯化反应为简单的取代反应。请你设想酯化反应的机理 。
2)酯化反应是一个可逆的反应,120 ℃时,平衡常数K= 。
(3)如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是________(填正确答案标号)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(4)浓硫酸与乙醇如何混合? 。
(5)控制滴加乙酸和乙醇混和液的速度等于蒸馏速度目的是? 。
(6)蒸出的粗乙酸乙酯中主要有哪些杂质? 。饱和的Na2CO3溶液洗涤除去乙酸。如何判断是否除净? 。用饱和NaCl溶液洗涤除去残留的Na2CO3溶液,为什么不用水? 。
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上学期摸底考试化学试卷(解析版) 题型:选择题
下列实验现象的叙述,正确的是 ( )
A.钠在氧气中燃烧,火焰呈黄色,产生Na2O固体
B.HClO见光分解生成H2O 和Cl2
C.钠投入水中,将沉入水底并熔化成小球、且有气泡产生
D.氯气通入紫色石蕊试液中,溶液先变红后褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com