
氮气与氢气反应生成氨气的平衡常数见下表:
|
|
N2+3H2 |
|||
|
温度 |
25℃ |
200℃ |
400℃ |
600℃ |
|
平衡常数K |
5×108 |
650 |
0.507 |
0.01 |
(1)工业上合成氨的温度一般控制在500℃,原因是 。
(2)在2 L密闭容器中加入1 mol氮气和3 mol氢气,进行工业合成氨的模拟实验,若2分钟后,容器内压强为原来的0.8倍,则0到2分钟,氨气的反应速率为________mol/(L·min)。
(3)下列说法能表明该反应达到平衡的是________
A.气体的平均分子量不再变化 B.密闭容器内的压强不再变化
C.v (N2) = 2 v (NH3) D.气体的密度不再变化
(4)下列措施,既能加快该反应的反应速率,又能增大转化率的是______________
A.使用催化剂 B.缩小容器体积 C.提高反应温度 D.移走NH3
(5)常温下,在氨水中加入一定量的氯化铵晶体,下列说法错误的是______。
A.溶液的pH增大 B.氨水的电离度减小 C.c(OH-)减小 D.c(NH4+)减小
(6)将氨水与盐酸等浓度等体积混合,下列做法能使c(NH4+)与c(Cl-)比值变大的是________
A. 加入固体氯化铵 B.通入少量氯化氢
C. 降低溶液温度 D.加入少量固体氢氧化钠
(1)催化剂的活性温度且反应速率较快(2分);
(2)0.2 mol/(L·min)(2分);
(3)AB(2分);
(4)B(2分) (5)AD(2分); (6)AC(2分)
【解析】
试题分析:(1)工业上合成氨的温度一般控制在500℃,原因主要是从反应的速率角度来考虑的,因为催化剂的活性温度且反应速率较快。
(2)N2+3H2  2NH3,设反应后氮气的物质的量为x,则氮气转化了1-x,氢气剩余3-(1-x),氨气生成2(1-x),根据压强之比和物质的量成正比,可得关系式4:【1-x+3-(1-x)+2(1-x)】=1:0.8。最终求得氨气的反应速率为0.2 mol/(L·min)。
2NH3,设反应后氮气的物质的量为x,则氮气转化了1-x,氢气剩余3-(1-x),氨气生成2(1-x),根据压强之比和物质的量成正比,可得关系式4:【1-x+3-(1-x)+2(1-x)】=1:0.8。最终求得氨气的反应速率为0.2 mol/(L·min)。
(3)合成氨气的反应,若没有达到平衡,反应前后平均分子质量始终发生变化,密闭容器内的压强也发生变化,而密度始终没有改变,故选AB。而C中v (N2) = 2 v (NH3) 没有说明反应的方向,无法做为判据。
(4)使用催化剂能加快速率但不能改变转化率,A错误;缩小容器体积两者都能实现,B正确;提高反应温度能加快速率但转化率降低,C错误;移走NH3 浓度降低,速率降低转化率增大,D错误
(5)根据氨水中存在的电离平衡可知,加入一定量的氯化铵晶体,增大了c(NH4+),平衡右移, 溶液的pH减小, A错误; 氨水的电离度减小,B正确; c(OH-)减小,C正确;c(NH4+)减大, D错误。
(6)将氨水与盐酸等浓度等体积混合,反应后生成氯化铵,此时溶液中存在NH4+的水解平衡, 加入固体氯化铵,增大了铵根浓度,抑制了其水解,比值增大, A正确。通入少量氯化氢,氯离子增大程度大于铵根的增大程度,B错误。 降低溶液温度,抑制其水解,铵根浓度增大, C正确。 加入少量固体氢氧化钠,铵根浓度减小,D错误。
考点:本题考查弱电解质的电离平衡和盐类水解平衡的移动问题。


 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
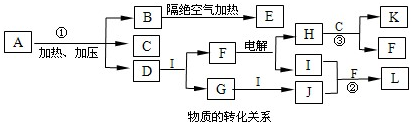


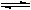 NH4++NH2-
NH4++NH2-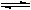 NH4++NH2-
NH4++NH2-查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| 催化剂 |
| 高温高压 |
| 催化剂 |
| 高温高压 |
| 原料 | 天然气 | 重油 | 煤 |
| 相对投资费用 | 1.0 | 1.5 | 2.0 |
| 能量消耗/J?t-1 | 28109 | 38109 | 48109 |
| ||
| 催化剂 |
| ||
| 催化剂 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:福建省上杭一中2010-2011学年高二下学期期中考试化学试题 题型:022
氮是地球上极为丰富的元素.填写下列空白.
(1)NH![]() 中N原子的杂化轨道类型为________,
中N原子的杂化轨道类型为________,
NH![]() 的空间构型为________.
的空间构型为________.
(2)常温下,锂可与氮气直接反应生成Li3N,Li3N晶体中氮以N3-存在,基态N3-的电子排布式为:________,Li3N晶体属于________晶体(填晶体类型).
(3)NH3的沸点为234K,NF3的沸点为154K,两者结构相似,NH3的沸点高于NF3的原因是:________.
(4)CO与N2相似,分子中都存在一个共价叁键,CO含________个π键.下表为CO与N2的相关信息.根据表中数据,说明CO比N2活泼的原因:________.

(5)根据下表数据,写出氮气与氢气反应生成氨气的热化学方程式________.
![]()
(6)CO与N2互为等电子体,其碳原子上有一对孤对电子,因此可作配体,如:Fe(CO)5、Ni(CO)4、Cr(CO)6等,在合成氨工业上中用铜洗液吸收CO,反应如下:

①基态Fe原子的未成对电子数有________个,
写出Cr、Cu+的价层电子排布式.________、________.
②醋酸二氨合铜(I)和醋酸羰基三氨合铜(I)都是配合物,[Cu(NH3)3CO]+中提供孤对电子的分子是:________,接受孤对电子的离子是:________,用箭号标出[Cu(NH3)2]+形成的配位键:________,[Cu(NH3)2]+中两个配位键的键角为180°,则Cu+采取________杂化与NH3形成配位键(填杂化类型).
③Ni(CO)4是无色液体,沸点42.1℃,熔点-19.3℃,难溶于水,易溶于有机溶剂.推测Ni(CO)4是________分子(填“极性”或“非极性”).
(7)氮化硅是一种高温陶瓷材料,它硬度大、熔点高、化学性质稳定.
①氮化硅晶体属于________晶体(填晶体类型);
②已知氮化硅晶体结构中,原子间都以共价键相连,且N原子与N原子,Si原子与Si原子不直接相连,同时每个原子都满足8电子结构,请写出氮化硅的化学式:________.
(8)极纯的氮气可由叠氮化钠(NaN3)加热分解而得到.2NaN3(s)=2Na(l)+3N2(g),反应过程中,断裂的化学键是离子键和共价键,形成的化学键有________.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com