
| A. | 无水硫酸铜、蔗糖 | B. | 硅胶、硫酸亚铁 | C. | 食盐、硫酸亚铁 | D. | 生石灰、食盐 |
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:多选题
| A. | 大多数有机物难溶于水,易溶于汽油、酒精、苯等有机溶剂;大多有机反应较慢,常伴有副反应发生,需催化 | |
| B. | 乙烯和苯分子中都有碳碳双键,分子中所有原子都共平面;溴苯、硝基苯、四氯化碳,它们的密度都比水大 | |
| C. | 乙烯和苯互为同系物 | |
| D. | 苯和四氯化碳都能使溴水褪色,都不能使酸性高锰酸钾溶液褪色;一定条件下,苯能与液溴或浓硝酸发生取代反应,也能与H2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
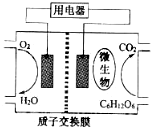 科学家近年来研制出一种新型细菌燃料电池.以葡萄糖为燃料的微生物燃料电池结构示意图如图所示.关于该电池的叙述正确的是( )
科学家近年来研制出一种新型细菌燃料电池.以葡萄糖为燃料的微生物燃料电池结构示意图如图所示.关于该电池的叙述正确的是( )| A. | 该电池的负极反应为O2+2H2O+4e-=4OH- | |
| B. | 电池的负极反应为:C6H12O6+6H2O=6CO2↑+24H++24e- | |
| C. | 放电过程中,H+从正极区向负极区迁移 | |
| D. | 在电池反应中,每消耗1mol氧气,理论上能生成标准状况下CO2气体22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2:二氧化锰和双氧水 带火星的木条 | |
| B. | Cl2:二氧化锰和浓盐酸 品红溶液 | |
| C. | CO2:大理石和稀硫酸 澄清石灰水 | |
| D. | NH3:NH4Cl固体和NaOH固体 湿润的红色石蕊试纸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该周期有32种元素 | |
| B. | 该周期的元素,原子序数最大为118 | |
| C. | 该周期的ⅦA族元素是金属元素 | |
| D. | 该周期的ⅢA族元素的氢氧化物具有两性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同体积,不同密度的N2和CO两种气体 | |
| B. | 相同密度的O2和O3两种气体 | |
| C. | 相同质量,不同密度的C2H4和C3H8两种气体 | |
| D. | 相同物质的量,不同体积的NH3和CH4两种气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
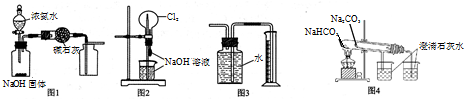
| A. | 图1装置可制取、收集干燥纯净的NH3 | |
| B. | 图2装置可以完成“喷泉”实验 | |
| C. | 图3装置可测量Cu 与浓硝酸反应产生气体的体积 | |
| D. | 图4装置可用比较NaHCO3和Na2CO3的热稳定性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


 ,D的化学名称是丙酮.
,D的化学名称是丙酮. .
. .
. (填结构简式).
(填结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (2)反应③中被氧化的物质与被还原的物质的物质的量之比为2:1
(2)反应③中被氧化的物质与被还原的物质的物质的量之比为2:1查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com